题目内容
mol是表示物质量的一种单位,1mol的Na、Mg、Al三种金属的质量分别为23克、24克、27克.室温时,向146克溶质质量分数为10%的盐酸溶液中分别加入两种金属M、N,先加入0.1mol的金属M,反应完毕后再加入0.2mol的金属N,则下列四组所加入的两种金属,放出气体总量最多的一组是
| 选项 | A | B | C | D |
| M | Na | Na | Al | Mg |
| N | Al | Mg | Na | Na |
- A.A
- B.B
- C.C
- D.D
C
分析:根据1mol的Na、Mg、Al三种金属的质量分别为23克、24克、27克,计算出0.1mol的金属M与0.2mol的金属N的实际的质量,然后找出酸和金属质量之间的关系,需要注意钠会与水反应进行分析.
解答:1mol的Na、Mg、Al三种金属的质量分别为23克、24克、27克,0.1mol的金属M与0.2mol的金属N质量在选项中分别为:
选项ABCDMNa:2.3克Na:2.3克Al:2.7克Mg:2.4克NAl:5.4克Mg:4.8克Na:4.6克Na:4.6克反应物、生成物间质量比:
Na~HCl~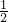 H2 Mg~2HCl~H2 Al~3HCl~
H2 Mg~2HCl~H2 Al~3HCl~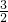 H2
H2
23 36.5 1 24 73 2 27 109.5 3
盐酸溶液中HCl总量为:14.6克,与A、B反应反应Mg、Al有剩余,产生H2各0.4克;与C反应Na有剩余,Na要与水反应产生氢气,因此氢气质量大于0.4克;从比例关系中可以看出,酸在D的反应,Na、Mg与HCl刚好完全反应,产生H2各0.4克,故选C.
点评:在解此类题时,首先分析各金属的性质,然后结合金属和酸反应之间的比例关系进行计算,需要注意有的活泼金属会与水反应生成氢气.
分析:根据1mol的Na、Mg、Al三种金属的质量分别为23克、24克、27克,计算出0.1mol的金属M与0.2mol的金属N的实际的质量,然后找出酸和金属质量之间的关系,需要注意钠会与水反应进行分析.
解答:1mol的Na、Mg、Al三种金属的质量分别为23克、24克、27克,0.1mol的金属M与0.2mol的金属N质量在选项中分别为:
选项ABCDMNa:2.3克Na:2.3克Al:2.7克Mg:2.4克NAl:5.4克Mg:4.8克Na:4.6克Na:4.6克反应物、生成物间质量比:
Na~HCl~
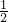 H2 Mg~2HCl~H2 Al~3HCl~
H2 Mg~2HCl~H2 Al~3HCl~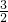 H2
H223 36.5 1 24 73 2 27 109.5 3
盐酸溶液中HCl总量为:14.6克,与A、B反应反应Mg、Al有剩余,产生H2各0.4克;与C反应Na有剩余,Na要与水反应产生氢气,因此氢气质量大于0.4克;从比例关系中可以看出,酸在D的反应,Na、Mg与HCl刚好完全反应,产生H2各0.4克,故选C.
点评:在解此类题时,首先分析各金属的性质,然后结合金属和酸反应之间的比例关系进行计算,需要注意有的活泼金属会与水反应生成氢气.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目