题目内容
【题目】石灰石是一种重要矿石,其主要成分为碳酸钙,在冶金、建材、化工等行业均有广泛用途.某校9年级科学探究小组的同学为了测定某种石灰石样品中碳酸钙的质量分数,设计了如下实验方案:取一定质量的石灰石样品与足量稀盐酸反应,测量反应后生成的CO2的体积,再将体积换算成质量,最后根据CO2的质量计算样品中碳酸钙的质量分数.下图Ⅰ为石灰石与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置.

(1)如图Ⅰ所示,因缺少长颈漏斗,同学们使用了一只普通漏斗,则需要加入较多的稀盐酸才能浸没漏斗下端管口,起到液封的作用.小明同学想到一个办法,他取来一支合适的试管,加装到装置中,既解决了液封问题,又减少了酸的用量.请你把小明加装试管的方法画在图中相应的位置(用签字笔或黑色钢笔画).
(2)检查图Ⅱ装置气密性的方法是 .
(3)在图Ⅱ装置中,油层的作用是 .
(4)反应结束后,读出量气管内水面上升的体积即为生成的CO2的体积.在读数前必须进行的一项操作是 .
【答案】(1)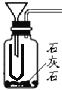 (2)用弹簧夹夹紧乳胶管,向量气 管中注入适量水,然后提高量气管,一段时间后,若量气管内液面不下降,说明装置的气密性良好;(3)防止CO2溶于水;(4)上下调节量气管高度,使装置两侧液面持平
(2)用弹簧夹夹紧乳胶管,向量气 管中注入适量水,然后提高量气管,一段时间后,若量气管内液面不下降,说明装置的气密性良好;(3)防止CO2溶于水;(4)上下调节量气管高度,使装置两侧液面持平
【解析】(1)将小试管加在漏斗的下面,故填:

(2)要检查装置2的气密性,可以用弹簧夹夹紧乳胶管,向量气 管中注入适量水,然后提高量气管,一段时间后,若量气管内液面不下降,说明装置的气密性良好,故填:用弹簧夹夹紧乳胶管,向量气 管中注入适量水,然后提高量气管,一段时间后,若量气管内液面不下降,说明装置的气密性良好;
(3)二氧化碳能溶于水,故油层能起到将水和二氧化碳隔绝,防止二氧化碳溶于水的作用,故填:防止CO2溶于水;
(4)要读出量气管内水面上升的体积即为生成的CO2的体积.在读数前必须上下调节量气管高度,使装置两侧液面持平.故填:上下调节量气管高度,使装置两侧液面持平.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究:
(1)将溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算所需浓盐酸和水的体积;
步骤2:根据计算结果,用 (填仪器名称)分别量取所需的浓盐酸和水;
步骤3:将浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
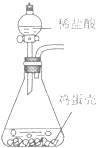
(2)测得各自的质量后,将鸡蛋壳置于如图所示的锥形瓶中,打开分液漏斗中的活塞,使其充分反应,直到不再产生气泡为止(假设装置中的稀盐酸足量,鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录如下表:(CaCO3+2HCl=CaCl2+H2O+CO2↑)
反应前 | 鸡蛋壳的质量 | 16克 |
装置和稀盐酸的总质量 | 220克 | |
反应后 | 装置及其内容物的总质量 | 231.6克 |
请计算该鸡蛋壳中碳酸钙的质量分数.