题目内容
航天飞机用金属铝和高氯酸铵(NH4ClO4)的混合物做固体燃料,加热铝粉使其被氧化放出大量的热,使混合物中的高氯酸铵分解,同时生成四种气体,两种是空气的主要成分,一种气体是氯气,还有一种是常见氧化物,因而产生巨大的推动力.试写出高氯酸铵受热分解的化学方程式 .
【答案】分析:由题意“高氯酸铵受热分解;同时生成四种气体,两种气体是空气中的主要成分,一种气体是氯气,还有一种气体是常见氧化物”则可推测知:反应物为高氯酸铵(NH4ClO4);生成物为氮气、氧气、氯气、水蒸气;反应条件为加热,故可书写化学方程式.
解答:解:由题意,先推测:两种气体是空气中的主要成分为氮气和氧气,常见的氧化物是水;又知其它生成物、反应条件,利用“定1法”对方程式进行配平,
可把NH4ClO4 的计量数定为1,故可书写化学方程式为2NH4ClO4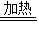 N2↑+2O2↑+Cl2↑+4H2O↑
N2↑+2O2↑+Cl2↑+4H2O↑
故答案为:2NH4ClO4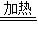 N2↑+2O2↑+Cl2↑+4H2O↑
N2↑+2O2↑+Cl2↑+4H2O↑
点评:根据信息书写方程式要根据题中信息确定反应物和生成物,反应条件,然后根据书写要求进行解答.
解答:解:由题意,先推测:两种气体是空气中的主要成分为氮气和氧气,常见的氧化物是水;又知其它生成物、反应条件,利用“定1法”对方程式进行配平,
可把NH4ClO4 的计量数定为1,故可书写化学方程式为2NH4ClO4
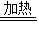 N2↑+2O2↑+Cl2↑+4H2O↑
N2↑+2O2↑+Cl2↑+4H2O↑故答案为:2NH4ClO4
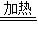 N2↑+2O2↑+Cl2↑+4H2O↑
N2↑+2O2↑+Cl2↑+4H2O↑点评:根据信息书写方程式要根据题中信息确定反应物和生成物,反应条件,然后根据书写要求进行解答.

练习册系列答案
相关题目