题目内容
下列是某位同学对阶段学习的有关内容的归纳,该同学归纳正确的个数为( )
①C﹣12原子和C﹣13原子不同的原因是它们的核内质子数不相同;
②空气质量级别从Ⅰ级到Ⅴ级,数字越大表示空气质量越好;
③KMnO4和K2MnO4中含有相同的原子团;
④燃烧需要同时满足三个条件,故破坏其中一个条件就可以灭火
⑤碳酸盐与酸反应有气体生成,则与酸反应产生气体的一定是碳酸盐;
⑥中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应
⑦碱性溶液能使酚酞溶液变红,则能使酚酞溶液变红的一定是碱性溶液
⑧某不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是Zn
A. 2个 B. 3个 C. 4个 D. 5个
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案为测定某地石灰石中碳酸钙的质量分数,某兴趣小组将一定质量的石灰石样品粉碎后分成两等份,进行如下实验:
(1)一份放于烧杯中,向烧杯中逐渐加入某一浓度的盐酸,反应过程测得剩余固体质量与加入盐酸的质量关系如图1所示(石灰石中的杂质不与盐酸反应,也不溶与水)。请回答下列问题:
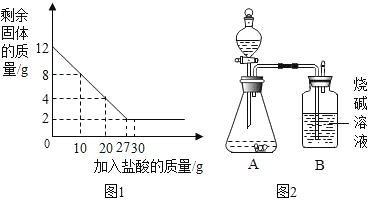
①石灰石样品中碳酸钙的质量分数_____;
②通过计算求所用盐酸的溶质质量分数。_____
(2)另一份进行如图2所示的实验:把产生的CO2气体用足量的烧碱溶液吸收,同时测量B瓶烧碱溶液增加的质量,结果如下表所示:
时间/分 | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
B增加的质量 | 0 | 2 | 3 | 4 | 4.6 | X | 4.6 |
①上表中,第5分钟时,x=_____;
②该实验测得样品中碳酸钙的质量分数_____(填大于、小于或等于)另一实验,其原因可能是_____。
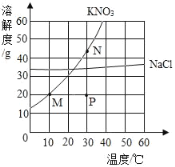
某化学兴趣小组在做“探究纯碱的性质”实验。
探究一:同学们做了如图所示的四组实验,并将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中。考试结束后,某兴趣小组发现大烧杯底部有沉淀,上层溶液呈红色。为了探究上层溶液的成分,进行了以下实验。

(提出问题)大烧杯中的上层溶液中除了含有水和酚酞外,还含有哪些离子?(假设难溶物质、水和酚酞均不会解离出离子)
(猜想假设)小明认为上层溶液中一定含有Na+、CO32﹣、H+、Cl﹣、Ba2+、Ca2+、OH﹣七种离子,你认为上层溶液中含有的离子最多可能有哪几种,它们分别是_____(填离子符号)。
(分析讨论)(1)小红认为上层溶液中一定不含有H+,因为上层溶液呈红色。请你分析上层溶液中不含有H+的另外一个理由_____。
(2)小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一定不含有CO32﹣.小红认为他的结论不正确,原因是_____。
(设计实验)为进一步确定上层溶液中是否含有CO32﹣,请你和小红一起参与下列探究:
实验操作 | 实验现象 | 实验结论 |
取大烧杯中上层溶液少许于一支试管中,滴加_____,静置 | ①_____ ②试管中的上层溶液仍是红色 | ①大烧杯中上层溶液中一定含有CO32﹣ ②同时还能得出大烧杯中的上层溶液中一定含有离子是_____(填离子符号) |
(实验结论)大烧杯中的上层溶液中一定含有的离子是_____(填离子符号)。
探究二:“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行测定。
(查阅资料)碱石灰是氧化钙与氢氧化钠固体的混合物,具有良好的吸水性还能吸收酸性气体;
(设计实验)根据如图的装置,他们设计了以下实验方案进行试验。

(1)如图装配好仪器,并检查装置气密性,准确称量5.0g的纯碱样品加入A中的锥形瓶,并在各装置中加入足量药品。
(2)打开止水夹K,先对装置A通入已除去氮气一会儿,再连接上装置B和C。
(3)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为_____。
(4)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入氮气一会儿。
(5)将反应后B装置内的混合物进行过滤,把获得的沉淀物进行、称量,利用沉淀物质量计算Na2CO3的质量分数。
(实验反思)
(1)实验设计中若没有装置C则本次测定的实验结果会_____(填“偏大”、“偏小”或“无影响”)
(2)老师在查看小组的实验设计后指出,该实验设计即使各步骤实验过程操作规范,测量数据准确,但最后的结果也会偏小,请你分析原因。_____。


 2nCH3CH2OH+2nCO2↑
2nCH3CH2OH+2nCO2↑ 占人体体重的10%(假设血液的密度是:1kg/L),则:
占人体体重的10%(假设血液的密度是:1kg/L),则:
 质量分数为50%的白酒的质量是多少?
质量分数为50%的白酒的质量是多少?