题目内容
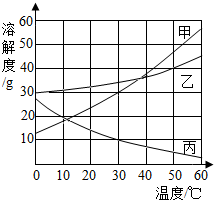 (2012?和平区二模)甲、乙、丙三种固体物质的溶解度曲线如图所示.
(2012?和平区二模)甲、乙、丙三种固体物质的溶解度曲线如图所示.(1)30℃时,丙的溶解度是
10g
10g
.(2)5℃时,取甲、乙、丙三种固体物质各20g分别加入盛有100g水的烧杯中,充分搅拌后得到的溶液,能够饱和的是
甲
甲
物质的溶液.又将三个烧杯的混合物温度都升高到30℃,所得到溶液溶质质量分数的大小关系是甲=乙>丙
甲=乙>丙
.(3)现有30℃的不饱和KNO3溶液,与该溶液有关的量有:①水的质量;②溶液中溶质KNO3的质量;③KNO3的质量分数;④30℃时KNO3的溶解度;⑤溶液的质量.用序号填空:
Ⅰ.在该不饱和溶液中加少量硝酸钾至饱和,不变的量有
①④
①④
;Ⅱ.将该不饱和溶液洹温蒸发至恰好饱和,不变的量有
②④
②④
.分析:根据固体物质的溶解度曲线可以:①查出某种物质在某温度下的溶解度,从而判断在一定量的溶剂中加入一定量的溶质形成的溶液是否达到饱和,②比较不同物质在同一温度下的溶解度的大小;加硝酸钾至饱和溶质增加,溶剂不变,温度不变溶解度不变;将该不饱和溶液恒温蒸发至饱和,溶剂减少,溶质不变,温度不变溶解度不变.
解答:解:(1)由丙的溶解度曲线可知,30℃时,丙的溶解度是 10g,
故答案为:10g.
(2)在5℃时,甲物质的溶解度小于20g,乙和丙物质的溶解度都大于20g,故甲能得到饱和溶液,乙和丙都不能形成饱和溶液,将温度升高到30℃时,甲和乙的溶解度都大于20g,溶质能全部溶解,丙的溶解度是10g,故丙物质不能全部溶解,所得溶液的溶质质量分数就是甲=乙>丙,
故答案为:甲=乙>丙
(3)Ⅰ.加硝酸钾至饱和溶质增加,溶剂不变,所以溶液质量增加,溶质质量分数增加,温度不变溶解度不变;Ⅱ.将该不饱和溶液恒温蒸发至饱和,溶剂减少,溶质不变,溶液质量减少,溶质质量分数增加,温度不变溶解度不变.
故答案为:(1)10g;
(2)甲;甲=乙>丙;
(3)①④;②④
故答案为:10g.
(2)在5℃时,甲物质的溶解度小于20g,乙和丙物质的溶解度都大于20g,故甲能得到饱和溶液,乙和丙都不能形成饱和溶液,将温度升高到30℃时,甲和乙的溶解度都大于20g,溶质能全部溶解,丙的溶解度是10g,故丙物质不能全部溶解,所得溶液的溶质质量分数就是甲=乙>丙,
故答案为:甲=乙>丙
(3)Ⅰ.加硝酸钾至饱和溶质增加,溶剂不变,所以溶液质量增加,溶质质量分数增加,温度不变溶解度不变;Ⅱ.将该不饱和溶液恒温蒸发至饱和,溶剂减少,溶质不变,溶液质量减少,溶质质量分数增加,温度不变溶解度不变.
故答案为:(1)10g;
(2)甲;甲=乙>丙;
(3)①④;②④
点评:本题难度不大,掌握不饱和溶液与饱和溶液之间的转化方法并能灵活运用是正确解答本题的关键

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目


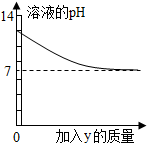 (2012?和平区二模)烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如下图所示.则符合该变化的一组物质是( )
(2012?和平区二模)烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如下图所示.则符合该变化的一组物质是( )