题目内容
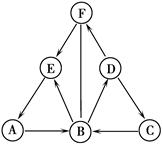
(4分)A、B、C、D、E为初中五种常见物质, 其中A是生活中最常见液体, B、D是气体,只有E含金属元素,B是常见单质(反应条件与其他物质均已略去)。“→”表示按方向一步转化,“——”表示两种物质间可以发生反应,所有反应都是初中常见反应。

⑴写出物质化学式:A: ,C: ;
⑵写出化学方程式:D+E 。

⑴写出物质化学式:A: ,C: ;
⑵写出化学方程式:D+E 。
⑴H2O H2SO4 ⑵CO2+Ca(OH)2==CaCO3↓+H2O
试题分析:A、B、C、D、E为初中五种常见物质, 其中A是生活中最常见液体,所以A是水,B、D是气体,且B能生成水,水也能生成B,所以B为氧气,D能与水反应,所以D是二氧化碳,D也能与E反应,二氧化碳还能与氢氧化钙反应,所以E是氢氧化钙,E能与C反应,所以C可能是酸,盐,C可由水反应生成,所以确定C应该是酸,而且是硫酸,B到C时亚硫酸氧化得到硫酸,A到C时三氧化硫和水反应生成硫酸,D和E的反应是CO2+Ca(OH)2==CaCO3↓+H2O。

练习册系列答案
相关题目