题目内容
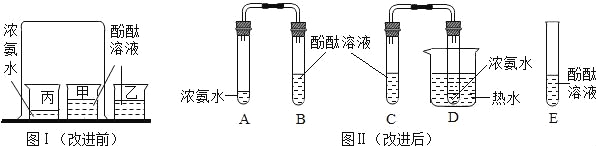
【题目】某化学兴趣小组利用如图装置探究制取气体的原理、方法及性质。结合装置图,回答下列问题:

(1)写出图中标号仪器的名称:a ,b 。
(2)向气体发生装置内加入药品前,必须 。
(3)用双氧水和二氧化锰制取氧气时,可选用的发生装置是 (填如图字母),若用高锰酸钾制氧气,选用的收集装置是 或E,用这种方法收集氧气需要验满,验满的方法是 。在 A 装置中的试管口还应放一团,这样做的目的是 。
(4)写出加热高锰酸酸钾制取氧气的化学表达式: 。
(5)导管口刚开始有气泡放出时,不宜立即收集,原因是 。
(6)某同学在实验过程中导致试管破裂,其原因可能有以下几种,你认为不正确的是 (填序号)。
A、加热时试管口向上
B、试管外壁有水,未擦干即加热
C、预热后,用酒精灯外焰对准受热部位加热
D、没有先将导管从水槽中取出便停止加热
(7)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,应选择的发生装置是 (填如图字母)。
【答案】
(1)长颈漏斗 锥形瓶
(2)检验装置气密性
(3)B C 把带火星的木条放在集气瓶口,木条复燃,证明集满 防止高锰酸钾粉末进入导管
(4)2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(5)刚开始排出的气体不纯(6)ABD(7)AD
【解析】
试题分析:
(1)通过分析题中所指仪器的作用可知,a是长颈漏斗,b是锥形瓶;
(2)向气体发生装置内加入药品前,必须检验装置气密性;
(3)实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,所以发生装置选B,氧气的密度比空气大,不易溶于水,所以选用的收集装置是C或E,氧气有助燃性,所以验满的方法是:把带火星的木条放在集气瓶口,木条复燃,证明集满,用高锰酸钾制取氧气时,试管口应放一团,目的是:防止高锰酸钾粉末进入导管;
(4)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(5)导管口刚开始有气泡放出时,不宜立即收集,原因是刚开始排出的气体不纯;
(6)A、根据加热时试管口向上,水会倒流炸裂试管,A正确;B、试管外壁有水,未擦干即加热会炸裂试管,B正确;C、预热后,用酒精灯外焰对准受热部位加热正确操作,不会导致试管破裂,C错误;D、没有先将导管从水槽中取出便停止加热,水会倒吸炸裂试管,D正确;故选:ABD;
(7)实验室制取氨气的反应物是固体,反应条件是加热氨气的密度比空气小,溶于水,所应选择的发生装置是AD。

【题目】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
假设:H2O2生成O2的快慢与催化剂种类有关。
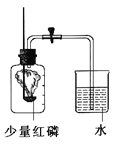
实验方案:常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
进行实验:如图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是: 。

实验记录:
实验编号 | 1 | 2 |
反应物 | 6% H2O2 | 6% H2O2 |
催化剂 | 1g 红砖粉 | 1g MnO2 |
时间 | 152s | 35s |
结论:该探究过程得出的结论是 。
反思:H2O2在常温下分解缓慢,加入MnO2或 红砖粉后反应明显加快,若要证明MnO2和 红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的 和 是否改变。