��Ŀ����
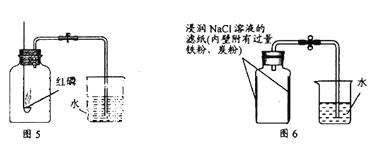
����Ŀ��ijУ��ѧѧϰС����ͼ1��ʾװ�õ��ˮ��Ϊ�ӿ������ʣ���С��ͬѧ�����˳���ʯ��ˮ����ˮ�����˵��ʵ�飬��ش��������⣺

��1���Թ�a������Ϊ______���Թ�b���ӵ��ǵ�Դ��______����
��2��ʵ��ʱ����ͬѧ����ʯī����Ϊ�缫���ڵ������з��ֳ���ʯ��ˮ������ˡ���Դ��쳣����С�����������̽����
��������룩��
�٣���������ˮ���ϼ��٣�������Һ�е��������Ʋ��ܼ����ܽ⣬�γɳ�����
�ڣ��������У��¶����ߣ�������Һ�е��������Ʋ����ܽ⣬�γɳ�����
������ʵ�飩��
�٣���ȡ��ͬŨ�ȡ�����ij���ʯ��ˮ������10mL����ˮ�����裬����ͬ��ѹ���ٴν��е��ʵ�飬�۲쵽��Һ��Ȼ�ǻ��ǵģ���˵����______��
�ڣ�ȡ100mL��ͬŨ�ȵij���ʯ��ˮ�ڴ��ձ��У����������ʵ��ʱ�������¶ȣ�û�й۲쵽���ǡ���˵����______��
�ۣ���С����ò��缫������ʯ��ˮ����ͼ3�����ֳ���ʯ��ˮû�б���ǣ������������ó���ʯ��ˮ����ǵ�ԭ�������______�йء�
�ܣ���ȡ���ǵ�Һ�壬�����м���ϡ���ᣬ���ö�����̼������������Ӧ�����Ķ�����̼Ũ�ȣ�����������ͼ3���ݴ��Ʋ�û�����Ӧ���У�______�����������ʵ�ԭ������ǣ�______��______�����û�ѧ����ʽ��ʾ��
�ݣ�ʵ�����ձ����ò�����ȷ����ʵ������и�С��ͬѧҲ���֣�����ǵ�Һ���еμ����ᣬ��û�����ݲ�������ԭ�������______��
���𰸡����� �� ��Һ����Dz������������������µ� ��Һ����Dz��������¶����ߵ��µ� ��ʯī����Ϊ�缫 ̼��� C+O2![]() CO2 Ca��OH��2+CO2�TCaCO3��+H2O ϡ������٣������Ժ��������Ʒ�Ӧ
CO2 Ca��OH��2+CO2�TCaCO3��+H2O ϡ������٣������Ժ��������Ʒ�Ӧ
��������
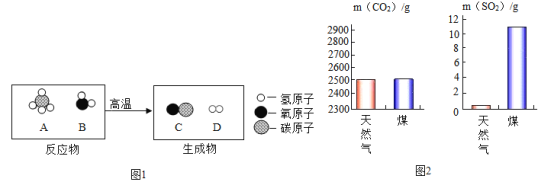
��1��ˮ��ͨ��������������������������������⣬�������1��2�������Թ�a�е�����Ϊ�������Թ�b���ӵ��ǵ�Դ��������
��2������ʵ�飺
������ͬ��ѹ���ٴν��е��ʵ�飬�۲쵽��Һ��Ȼ�ǻ��ǵģ���˵������Һ����Dz������������������µģ�
���������Ƶ��ܽ�����¶ȵ����߶���С������ȡ100mL��ͬŨ�ȵij���ʯ��ˮ�ڴ��ձ��У����������ʵ��ʱ�������¶ȣ�û�й۲쵽���ǣ���˵������Һ����Dz��������¶����ߵ��µģ�
�۲��ò��缫������ʯ��ˮ�����ֳ���ʯ��ˮû�б���ǣ�����ó���ʯ��ˮ����ǵ�ԭ���������ʯī����Ϊ�缫�йأ�
����ͼ��ʾ������ϡ����ļ��룬������̼Ũ������Ʋ�û�����Ӧ���У�̼��ƣ�̼�������ڵ�ȼ�����������ɶ�����̼��������̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ�����Բ��������ʵ�ԭ������ǣ�C+O2![]() CO2��Ca��OH��2+CO2�TCaCO3��+H2O��
CO2��Ca��OH��2+CO2�TCaCO3��+H2O��
������ǵ�Һ���еμ����ᣬ��û�����ݲ�����ԭ������ǣ�ϡ������٣������Ժ��������Ʒ�Ӧ��

 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
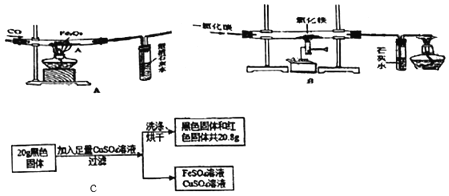
ͬ������ϵ�д�����Ŀ��������ʵ���ҽ���CO��ԭ��������ʵ����þƾ��Ƽ��ȣ�ͼA�����鱾ʵ�飨ͼB��������ͬ�������ڵõ��ĺ�ɫ��ĩ�м�ϡ���ᣬû�����ݲ�����������ͼAʵ���з�Ӧ��õ��ĺ�ɫ��ĩ�ijɷֽ���������̽����
���������ϣ������ۼ����ļ��ֳ������������ɫ���������ʡ�
���� | ���� | Fe2O3 | Fe3O4 | FeO |
��ɫ | ��ɫ | ����ɫ | ��ɫ | ��ɫ |
�ܷ������� | �� | ���� | �� | ���� |
��ʵ���Ҿƾ��Ƶ��¶�Ϊ400��500�棬�ƾ���Ƶļ����¶���1000�����ҡ�
�۵��¶ȸ���300�����ϣ�Fe2O3���ױ���ԭ��Fe3O4�����¶ȸ���600�����ϣ�Fe3O4���ױ���ԭFeO�����¶ȸ���700�����ϣ�FeO���ױ���ԭ��Fe��
��������⣩ͼAʵ��õ���ɫ��ĩ�ijɷ���ʲô��
��������룩��ɫ��ĩ�ijɷ��ǣ���FeO��Fe3O4��FeO��Fe3O4����FeO��Fe3O4��Fe2O3��
�����������ۣ�����_____����������_____��
��1��װ��A��һ�����Դ��ô�����_____��
��2����д������ʯ��ˮ�з����ķ�Ӧ�Ļ�ѧ����ʽ_____��
��3���ɶԱ�ʵ���֪����ԭ��������ʵ�������_____�йء�
��ʵ����ƣ���ͼAʵ��õ���ɫ��ĩ����һ�������У��ô����Ӵ���ɫ��ĩ������_____����˵���������ȷ��
��4��ʵ��B���õ��ĺ�ɫ���������Fe��Fe3O4���е�һ�ֻ����֡�С���������ʵ��̽����ɷ֣����������ɸ�̽�����̡�
��̽�����̣��ٶ����о���ȡ������ͼBʵ��õ��ĺ�ɫ��ĩ��һ�Թ��У���������������ͭ��Һ�����������_____����֤����ɫ������������
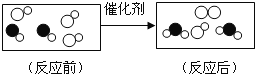
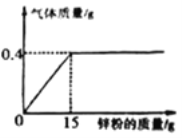
�ڶ����о���ȡBʵ��õ��ĺ�ɫ����20g�������ͼCʵ�飺���Ʋ��ɫ����ijɷ���_____��
����ͬѧ��ͼͨ����Ӧǰ����������ı仯��ȷ����ɫ����ijɷ֣�����Ϊ�����𣿣������������ڷ�Ӧ����ȫ��Ӧ��_____����������������������������_____��