题目内容
【题目】配平下面方程式:
(1)_____Cu2(OH)2CO3![]() _____CuO+_____CO2+_____H2O
_____CuO+_____CO2+_____H2O
(2)_____KMnO4![]() _____K2MnO4+_____MnO2+_____O2
_____K2MnO4+_____MnO2+_____O2
(3)_____Al+_____Fe3O4![]() _____Fe+_____Al2O3
_____Fe+_____Al2O3
(4)_____Al+_____H2SO4=_____Al2(SO4)3+_____H2
(5)_____Al(OH)3+_____HCl=_____AlCl3+_____H2O
(6)_____C22H46+_____O2![]() _____CO2+_____H2O
_____CO2+_____H2O
【答案】1 2 1 1 2 1 1 1 8 3 9 4 2 3 1 3 2 6 2 3 2 67 44 46
【解析】
(1)用观察法,将“CuO”的计量数配成“2”即可,该反应的化学方程式为Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O。
2CuO+CO2↑+H2O。
(2)用定一法:把方程式中较复杂的化学式前的系数定为“1”,该反应的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(3)利用奇数配偶法,先配平氧元素,再配平铁、铝元素,该反应的化学方程式为8Al+3Fe3O4![]() 9Fe+4Al2O3。
9Fe+4Al2O3。
(4)用定一法:把方程式中较复杂的化学式前的系数定为“1”,该反应的化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑。
(5)用观察法配平,先在“HCl”的前边配计量数“3”,再在“H2O”的前边计量数配“3”,该反应的化学方程式为:2Al(OH)3+6HCl=2AlCl3+3H2O。
(6)用定一法:把方程式中较复杂的化学式前的系数定为“1”,该反应的化学方程式为:2C22H46+67O2![]() 44CO2+46H2O。
44CO2+46H2O。

【题目】根据下表回答问题:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
NH4Cl | 33.5 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
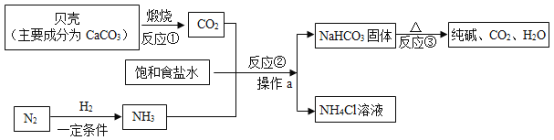
(1)海水中含有大量的氯化钠,海水晒盐的原理是___________,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是_____________,可向滤出晶体后的NaHCO3溶液中加入________以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在________℃之间。
(3)如图中,A是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到固体。

I.C中溶液的质量是________g。A溶液为NH4Cl的__________(选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为___________(结果精确到0.1%)。
II.对以上过程的分析,正确的是______(选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
③由B到C开始析出NH4Cl固体的温度在40℃至50℃之间
【题目】化学反应的程度与反应物的浓度之间有一定的规律可循。某实验小组各取等质量的木炭和等质量的硫分别在容积相同的集气瓶中燃烧。记录如下:
实验 | 实验步骤 | 实验现象 | 燃烧反应的化学符号表达式 | |
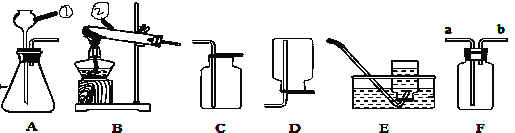
A | ①木炭在空气中燃烧 | ①木炭红热 | 产生的气体都能使澄清石灰水变浑浊 | _____ |
②木炭在氧气中燃烧 | ②_____ | |||
B | ③硫在空气中燃烧 | ③_____ | 产生的气体都有刺激性气味 | _____ |
④硫在氧气中燃烧 | ④明亮的蓝紫色火焰 | |||
通过A、B两组对比实验的现象,可以得出的规律是:_____。