题目内容
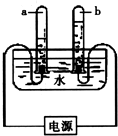
下列关于电解水实验的叙述正确的是( )
分析:电解水,发生反应的化学方程式为:2H2O
2H2↑+O2↑;可观察到:与电源负极相连的一边产生较多的气体,该气体燃烧火焰呈淡蓝色,罩在火焰上方冷而干燥的烧杯壁有水出现,可说明为氢气;与电源正极相连的一边产生气体可以使带火星的木条复燃,可说明为氧气;两边气体体积比为2:1,质量之比为8:1;由实验可得出水由氢氧元素组成的结论;根据以上现象或结论,对题中叙述进行判断,选出正确的判断.
| ||
解答:解:A、电解水的反应是由一种物质生成了两种物质,该反应属于分解反应.故A错误;
B、正负电极上产生的气体质量之比为8:1.故B错误;
C、负极产生的气体是氢气,能燃烧.故C错误;
D、电解水生成了氢气和氧气,说明水是由氢元素和氧元素组成的.故D正确.
故选D.
B、正负电极上产生的气体质量之比为8:1.故B错误;
C、负极产生的气体是氢气,能燃烧.故C错误;
D、电解水生成了氢气和氧气,说明水是由氢元素和氧元素组成的.故D正确.
故选D.
点评:题目比较简单,主要根据所学的有关电解水的实验的知识,经过合理的分析结合对该实验的记忆即可判断正误.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 (2013?锦州)下列关于电解水实验的叙述正确的是( )
(2013?锦州)下列关于电解水实验的叙述正确的是( )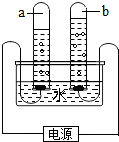 如图所示,下列关于电解水实验的叙述正确的是( )
如图所示,下列关于电解水实验的叙述正确的是( )