题目内容
长期呼吸PM2.5超标的空气,对人体的健康会产生严重的危害.PM2.5中的颗粒成分复杂,硝酸盐颗粒和硫酸盐颗粒(主要以硝酸按和硫酸按的形式存在)是其中的主要成分.小明想用化学方法大致测定PM2.5中硝酸按和硫酸按的含量高低,他将采集PM2.5的滤膜用一定量的蒸馏水充分洗涤,将洗涤液分为等量的V1,V2两份.(1)先往洗涤液V1中加入足量的硝酸钡溶液,得到硫酸钡沉淀M克.洗涤液V1中硫酸按的质量是多少克?(列式计算,相对原子质量:(H-l; N-14; S-32; 0-16; Ba-137)
(2)再往洗涤液V2中加入足量的氢氧化钠,并加热,收集到氨气N克.(不考虑氨气溶解)
已知:NH4 NO3+NaOH
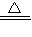 NaNO3+H2O+NH3↑;
NaNO3+H2O+NH3↑;(NH4)2SO4+2NaOH
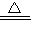 Na2SO4+2H2O+2NH3↑
Na2SO4+2H2O+2NH3↑若要知道洗涤液V2中硝酸铵的质量,下一步计算需要先求出______的质量.
【答案】分析:硝酸铵不能和硝酸钡反应,通过硫酸铵和硝酸钡反应生成的硫酸钡的质量,可以求出硫酸铵的质量;
根据硫酸铵和氢氧化钠反应生成氨气的质量,可以求出硝酸铵和氢氧化钠反应生成氨气的质量,进一步可以求出硝酸铵的质量.
解答:解:(1)设洗涤液V1中硫酸铵的质量为X,
(NH4)2SO4+Ba(NO3)2═BaSO4↓+2NH4NO3
132 233
X M克
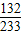 =
=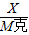
X=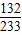 M克;
M克;
答:洗涤液V1中硫酸铵的质量为 M克.
M克.
(2)硫酸铵和硝酸铵都能够与氢氧化钠反应生成氨气,总质量是N克,
在(1)中,已经求出硫酸铵的质量,可以根据硫酸铵和氢氧化钠反应的化学方程式求出生成氨气的质量,
那么硝酸铵和氢氧化钠反应生成的氨气的质量就可以求出,从而进一步求出硝酸铵的质量.
故填:硫酸铵和氢氧化钠溶液反应生成氨气.
点评:本题比较容易,应该注意的是如何求洗涤液V2中,硝酸铵与氢氧化钠溶液反应生成的氨气的质量.
根据硫酸铵和氢氧化钠反应生成氨气的质量,可以求出硝酸铵和氢氧化钠反应生成氨气的质量,进一步可以求出硝酸铵的质量.
解答:解:(1)设洗涤液V1中硫酸铵的质量为X,
(NH4)2SO4+Ba(NO3)2═BaSO4↓+2NH4NO3
132 233
X M克
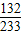 =
=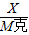
X=
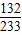 M克;
M克;答:洗涤液V1中硫酸铵的质量为
 M克.
M克.(2)硫酸铵和硝酸铵都能够与氢氧化钠反应生成氨气,总质量是N克,
在(1)中,已经求出硫酸铵的质量,可以根据硫酸铵和氢氧化钠反应的化学方程式求出生成氨气的质量,
那么硝酸铵和氢氧化钠反应生成的氨气的质量就可以求出,从而进一步求出硝酸铵的质量.
故填:硫酸铵和氢氧化钠溶液反应生成氨气.
点评:本题比较容易,应该注意的是如何求洗涤液V2中,硝酸铵与氢氧化钠溶液反应生成的氨气的质量.

练习册系列答案
相关题目
 NaNO3+H2O+NH3↑;
NaNO3+H2O+NH3↑; NaNO3+H2O+NH3↑;
NaNO3+H2O+NH3↑; NaNO3+H2O+NH3↑;
NaNO3+H2O+NH3↑;