题目内容
【题目】废旧金属可回收利用,用合金废料(含Fe、Cu和Al)制取FeSO4溶液和回收金属Cu。实验流程如下图所示(部分生成物已略):
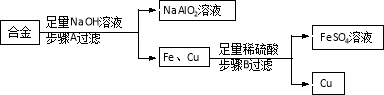
(1)合金属于____________(填“纯净物”或“混合物”)。
(2)生活中铝比铁更耐腐蚀的原因____________(用化学反应方程式解释)。
(3)步骤A化学反应方程式表示为:2A1+2NaOH+2R=2NaA1O2+3H2↑,依据质量守恒定律推出R的化学式为_____________________。
(4)步骤B发生的化学反应方程式为__________________________;反应的基本类型为___________。
【答案】(1)混合物;(2)4A1+3O2==== 2A12O3;(3)H2O(4)Fe+ H2SO4 == FeSO4 + H2↑;置换反应;
【解析】(1)在一种金属中加入融合了其它的金属或非金属形成的具有金属特性的物质叫合金。由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;(2)生活中铝比铁更耐腐蚀的原因是铝和空气中的氧气缓慢反应生成致密的氧化铝薄膜,阻止铝的进一步锈蚀;反应方程式为:4A1+3O2==== 2A12O3;(3)步骤A化学反应方程式表示为:2A1+2NaOH+2R=2NaA1O2+3H2↑,据质量守恒定律可知,化学反应前后原子的种类、个数不变,反应前有2个氧原子、2个铝原子、 2个氢原子、2个钠原子,反应后有4个氧原子、2个铝原子、6个氢原子、2个钠原子,所以一个X的分子中有2个氧原子、1个氢原子;X的化学式为H2O(4)步骤B中,发生的化学反应是铁与硫酸反应生成硫酸亚铁和氢气,方程式为Fe+ H2SO4 == FeSO4 + H2↑;一种单质和一种化合物生成另一种单质和另一种化合物的反应叫置换反应;

