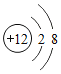题目内容
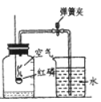
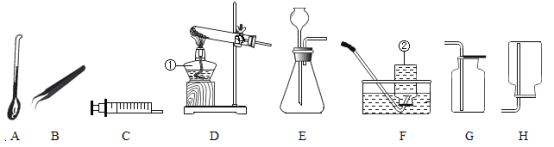
【题目】实验室部分装置如图所示,请回答下列问题。
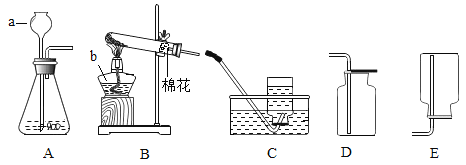
(1)仪器a的名称是________
(2)写出反应的表达式,并选择发生和收集氧气的装置,填写在下表中(填字母)。
选用药品 | 化学反应符号表达式 | 发生装置 | 收集装置 |
高锰酸钾 | _________________________ | 不填 | 不填 |
过氧化氢 | _________________________ | ________ | ________ |
(3)如何验证一瓶气体是否为氧气?___________________________。
(4)如果用固体锌与硫酸溶液常温下制备氢气。可选用的发生装置是_________(填字母)。若改用如图装置收集氢气(氢气难溶于水),则气体应从______进(填“a”或“b”)。
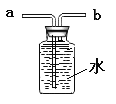
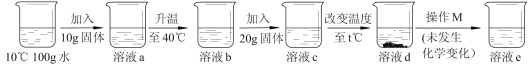
(5)a和b为质量相等的两份固体,a为混有二氧化锰的氯酸钾,b为氯酸钾。分别同时加热a和b至完全反应,下列图像能正确表示氧气的质量随时间变化关系的是(_____)
A B
B C
C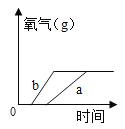 D
D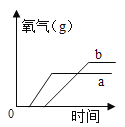
【答案】长颈漏斗 ![]()
![]() A D 将带火星的木条伸入集气瓶,木条复燃则瓶内气体为氧气,否则不是氧气 A b D
A D 将带火星的木条伸入集气瓶,木条复燃则瓶内气体为氧气,否则不是氧气 A b D
【解析】
(1)仪器a为长颈漏斗;
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应符号表达式不需配平,故为![]() ;过氧化氢在二氧化锰的催化下生成水和氧气,反应符号表达式为
;过氧化氢在二氧化锰的催化下生成水和氧气,反应符号表达式为![]() ;该反应的反应物为液体和固体,且不需要加热,则反应仪器应为固液不加热型,为A;生成的氧气不易溶于水,密度比空气大,可以选择排水集气法或向上排空气法收集,即C或D;
;该反应的反应物为液体和固体,且不需要加热,则反应仪器应为固液不加热型,为A;生成的氧气不易溶于水,密度比空气大,可以选择排水集气法或向上排空气法收集,即C或D;
(3)验证氧气的方法为:将带火星的木条伸入集气瓶,木条复燃则瓶内气体为氧气,否则不是氧气;
(4)锌为固体,硫酸溶液为液体,反应不需加热,所以选固液不加热型反应装置A;不论哪种气体,其密度均小于水,故若用如图所示装置收集,均应从“b”导管进气;
(5)按题目要求,a份为二氧化锰和氯酸钾的混合物,b份为氯酸钾纯净物。加热后,a份二氧化锰又作为氯酸钾的催化剂;而b份为纯净氯酸钾,没有催化剂,所以比较反应速率为a快于b。但a份中有部分是二氧化锰,二氧化锰是催化剂,不影响氧气的量,而b份全部是氯酸钾,故生成氧气的质量应a<b。综上所述,应选填D。
故答案为:长颈漏斗;![]() ;
;![]() ;A;D;将带火星的木条伸入集气瓶,木条复燃则瓶内气体为氧气,否则不是氧气;A;b;D
;A;D;将带火星的木条伸入集气瓶,木条复燃则瓶内气体为氧气,否则不是氧气;A;b;D

 阅读快车系列答案
阅读快车系列答案【题目】(一)下图所示是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷(白磷的着火点40摄氏度),将它放在盛有沸水的烧杯上方,进行试验。请完成下图所示实验报告。
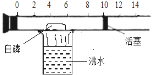
(1)实验目的:______________
(2)实验现象: ①玻璃容器内___________,②活塞_________ ,③活塞最后停在刻度______ 附近
(3)实验结论:空气的成分按体积计算,氧气约占空气体积的五分之一。
(二)学校化学兴趣小组的同学知道二氧化锰能作过氧化氢分解的催化剂以后,想再探究其他一些物质如氧化铝(Al2O3)是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白:
(1)〔问题〕Al2O3能不能作过氧化氢分解的催化剂呢?
(2)〔猜想〕Al2O3能作过氧化氢分解的催化剂。
(3)〔实验验证〕
实验步骤 | 实验现象 | 实验结论 | |
实验一 | ____________ | 木条不复燃 | 常温下过氧化氢溶液的分解速率很慢 |
实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,将带火星的木条伸入试管中 | 木条复燃 | Al2O3能加快过氧化氢的分解速率 |
(4)〔结论〕Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
(5)〔讨论与反思〕经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验(实验三):
〔实验目的〕 探究_________。
〔实验步骤〕 ①准确称量少量Al2O3 的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、烘干、_________;④反应前后进行对比。
〔讨论〕如果Al2O3在反应前后_________不变,_______(“已能”或“还不能”)说明Al2O3可以作过氧化氢分解的催化剂。
理由是:_________