题目内容
在实验室中小揭同学在相同温度下,取大小相同、表面光亮的Fe、Mg、Zn、Cu四种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中验证金属的活动性,现象如图.小阳同学将铁粉加入到硫酸铜溶液中,实验后发现只有一种紫红色金属.请回答:

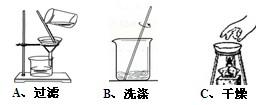
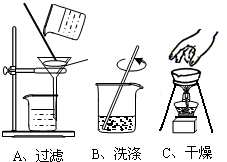
(1)如图是回收该金属的实验操作:操作中有一处错误,指出错误________.
(2)从化学性质上看,与盐酸反应最剧烈 的金属是________,这四种金属中,有一种金属的盐溶液能与其他三种金属发生反应,该金属 是________.
(3)性质决定用途,用途反映性质是重要的化学学科思想.用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的________性.
(4)小普同学为了验证金属铬的活动性,他也在相同温度下,取大小相同、表面光亮的Cr、Mg两种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
| 金属 | Cr | Mg |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
②小宁尝试将铬片放入硫酸铜溶液中,你认为会反应吗?能反应请写出Cr跟CuSO4溶液反应的化学方程式,不能请说明理由?________.
解:(1)在进行干燥操作中,干燥完毕应使用坩埚钳取下加热后蒸发皿而不能用手直接取下;故答案为:用手拿加热的蒸发皿或没用坩埚钳夹持蒸发皿
(2)根据金属活动性强弱关系镁>锌>铁>氢>铜,镁、锌、铁可与盐酸反应,且金属性越强与酸反应速度越快,强金属能置换出弱金属;故答案为:镁、铜
(3)镁能在空气中燃烧,生成氧化镁;故答案为:可燃性
(4)由于金属镁与盐酸反应产生气泡的速度明显快于铬,根据产生气泡的速度越快则该金属活动性越强,镁的活动性大于铬大于铜,且反应中Cr显+2价,故答案为:①Mg、Cr、Cu ②Cr+CuSO4=CrSO4+Cu
分析:(1)观察操作装置图,根据图示操作的要求,判断图示操作中的错误;
(2)根据金属活动性强弱关系镁>锌>铁>氢>铜,由放入盐酸中的四种金属与盐酸反应情况推测即可,
(3)镁能在空气中燃烧,生成氧化镁;
(4)通过实验来验证金属活动性顺序.根据金属单质和盐溶液的反应规律,确定生成物的组成.根据金属与盐酸反应的现象,利用探究资料所提供的判断依据,判断金属的活动性;
点评:本题主要考查如何设计实验,进行实验,并能正确分析,得出科学的结论的内容.金属活动性顺序中位于氢之前的金属能从酸中置换出氢,在相同条件下,金属活动性越强,与酸反应产生气泡的速度越快.
(2)根据金属活动性强弱关系镁>锌>铁>氢>铜,镁、锌、铁可与盐酸反应,且金属性越强与酸反应速度越快,强金属能置换出弱金属;故答案为:镁、铜
(3)镁能在空气中燃烧,生成氧化镁;故答案为:可燃性
(4)由于金属镁与盐酸反应产生气泡的速度明显快于铬,根据产生气泡的速度越快则该金属活动性越强,镁的活动性大于铬大于铜,且反应中Cr显+2价,故答案为:①Mg、Cr、Cu ②Cr+CuSO4=CrSO4+Cu
分析:(1)观察操作装置图,根据图示操作的要求,判断图示操作中的错误;
(2)根据金属活动性强弱关系镁>锌>铁>氢>铜,由放入盐酸中的四种金属与盐酸反应情况推测即可,
(3)镁能在空气中燃烧,生成氧化镁;
(4)通过实验来验证金属活动性顺序.根据金属单质和盐溶液的反应规律,确定生成物的组成.根据金属与盐酸反应的现象,利用探究资料所提供的判断依据,判断金属的活动性;
点评:本题主要考查如何设计实验,进行实验,并能正确分析,得出科学的结论的内容.金属活动性顺序中位于氢之前的金属能从酸中置换出氢,在相同条件下,金属活动性越强,与酸反应产生气泡的速度越快.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(2011?揭阳模拟)在实验室中小揭同学在相同温度下,取大小相同、表面光亮的Fe、Mg、Zn、Cu四种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中验证金属的活动性,现象如图.小阳同学将铁粉加入到硫酸铜溶液中,实验后发现只有一种紫红色金属.请回答:

(1)如图是回收该金属的实验操作:操作中有一处错误,指出错误.

(2)从化学性质上看,与盐酸反应最剧烈 的金属是,这四种金属中,有一种金属的盐溶液能与其他三种金属发生反应,该金属 是.
(3)性质决定用途,用途反映性质是重要的化学学科思想.用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的性.
(4)小普同学为了验证金属铬的活动性,他也在相同温度下,取大小相同、表面光亮的Cr、Mg两种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
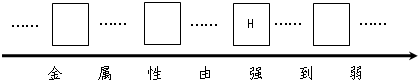
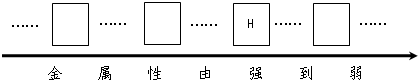
①请将铬、镁、铜三种金属的元素符号 填写在下列金属活动性顺序表中的相应位置.

②小宁尝试将铬片放入硫酸铜溶液中,你认为会反应吗?能反应请写出Cr跟CuSO4溶液反应的化学方程式,不能请说明理由?.

(1)如图是回收该金属的实验操作:操作中有一处错误,指出错误.

(2)从化学性质上看,与盐酸反应最剧烈 的金属是,这四种金属中,有一种金属的盐溶液能与其他三种金属发生反应,该金属 是.
(3)性质决定用途,用途反映性质是重要的化学学科思想.用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的性.
(4)小普同学为了验证金属铬的活动性,他也在相同温度下,取大小相同、表面光亮的Cr、Mg两种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
| 金属 | Cr | Mg |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |

②小宁尝试将铬片放入硫酸铜溶液中,你认为会反应吗?能反应请写出Cr跟CuSO4溶液反应的化学方程式,不能请说明理由?.