题目内容
Na2CO3是一种白色粉末,可以跟CO2和H2O反应生成NaHCO3,该反应的化学方程式为
Na2CO3+H2O+CO2=2NaHCO3
Na2CO3+H2O+CO2=2NaHCO3
;Na2CO3与稀盐酸反应放出CO2,写出反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
,但实验室却不用这个反应制备CO2,其主要原因可能是:反应速率太快,无法控制反应的进行
反应速率太快,无法控制反应的进行
;已知Na2CO3的溶解度比NaHCO3大,那么在饱和的Na2CO3溶液中连续通入CO2,可观察到的现象是:有白色固体析出
有白色固体析出
.分析:根据题干叙述进行分析,碳酸钠能与二氧化碳和水反应生成碳酸氢钠;碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,此反应速率快;在溶液中产生溶解度较小的物质,会析出固体,据此解答.
解答:解:碳酸钠能与二氧化碳和水反应生成碳酸氢钠;碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,此反应速率快,不利于控制反应的进行;在饱和的碳酸钠溶液中连续通入二氧化碳,会生成碳酸氢钠,由于碳酸氢钠的溶解度小于碳酸钠,会析出碳酸氢钠的固体,故填:Na2CO3+H2O+CO2=2NaHCO3,Na2CO3+2HCl=2NaCl+H2O+CO2↑,反应速率太快,无法控制反应的进行,有白色固体析出.
点评:本题考查了常见化学方程式的书写以及与溶解度的有关知识,完成此题,可以依据已有的知识进行.书写反应的化学方程式要注意配平.

练习册系列答案
相关题目
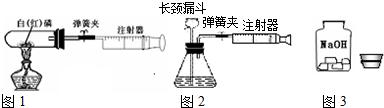


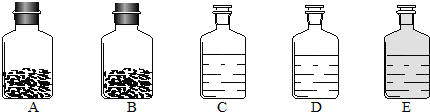
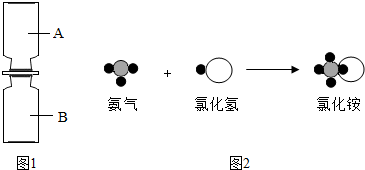 (2012?连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“
(2012?连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“ ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图2表示.
”表示氯原子,上述反应过程可用图2表示.