题目内容
 (2013?朝阳区二模)现有失去标签的5种无色溶液,分别是Na2CO3、NaCl、Ca(OH)2、NaOH和稀盐酸,任取其中的4种贴上A、B、C、D标签,进行如下实验.
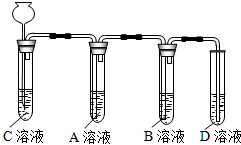
(2013?朝阳区二模)现有失去标签的5种无色溶液,分别是Na2CO3、NaCl、Ca(OH)2、NaOH和稀盐酸,任取其中的4种贴上A、B、C、D标签,进行如下实验. (1)依据如图装置进行实验,其中夹持固定装置已略去.从长颈漏斗加入稀盐酸,可以观察到C溶液中有气泡产生,A溶液中有白色沉淀生成,B、D溶液均无明显变化.则C溶液与稀盐酸反应的化学方程式为
Na2CO3+2HCl═2NaCl+CO2↑+H2O
Na2CO3+2HCl═2NaCl+CO2↑+H2O
;A溶液中发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
.(2)取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热.再取少量D溶液倒入另一蒸发皿,加热,有白色固体析出,停止加热.则B是
稀盐酸
稀盐酸
.(3)同学们认为实验(1)反应后的D溶液中溶质的成分有多种可能,请你设计实验方案证明
取反应后的D溶液于试管中,滴加过量的氯化钙溶液,若无白色沉淀则溶液中溶质为NaCl;若有白色沉淀.继续向上层清液中加入无色酚酞,若酚酞变红,则溶液中的溶质为NaOH和Na2CO3,若酚酞不变红,则溶液中的溶质为Na2CO3
取反应后的D溶液于试管中,滴加过量的氯化钙溶液,若无白色沉淀则溶液中溶质为NaCl;若有白色沉淀.继续向上层清液中加入无色酚酞,若酚酞变红,则溶液中的溶质为NaOH和Na2CO3,若酚酞不变红,则溶液中的溶质为Na2CO3
.分析:根据已有知识进行分析,碳酸钠能与盐酸反应生成二氧化碳气体,二氧化碳能使澄清的石灰水变浑浊,据此解答.
解答:解:
(1)从长颈漏斗中加入盐酸,C中产生气泡,说明C中盛有的是碳酸钠溶液,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,产生的二氧化碳倒入A中产生白色沉淀,说明A中盛有的是氢氧化钙溶液,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,故填:Na2CO3+2HCl═2NaCl+CO2↑+H2O,CO2+Ca(OH)2=CaCO3↓+H2O;
(2)盐酸是氯化氢的水溶液,气体的溶解度随温度的升高而减小,当加热B中溶液会闻到刺激性气味,说明溶解在水中的氯化氢由于温度升高而逸出,故填:稀盐酸;
(3)D中原来可能盛有的是氯化钠溶液,也可能是盛有的氢氧化钠溶液,氢氧化钠会与二氧化碳反应生成碳酸钠,故可以取反应后的D溶液于试管中,滴加过量的氯化钙溶液,若无白色沉淀则溶液中溶质为NaCl;若有白色沉淀.继续向上层清液中加入无色酚酞,若酚酞变红,则溶液中的溶质为NaOH和Na2CO3,若酚酞不变红,则溶液中的溶质为Na2CO3,故填:取反应后的D溶液于试管中,滴加过量的氯化钙溶液,若无白色沉淀则溶液中溶质为NaCl;若有白色沉淀.继续向上层清液中加入无色酚酞,若酚酞变红,则溶液中的溶质为NaOH和Na2CO3,若酚酞不变红,则溶液中的溶质为Na2CO3.
(1)从长颈漏斗中加入盐酸,C中产生气泡,说明C中盛有的是碳酸钠溶液,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,产生的二氧化碳倒入A中产生白色沉淀,说明A中盛有的是氢氧化钙溶液,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,故填:Na2CO3+2HCl═2NaCl+CO2↑+H2O,CO2+Ca(OH)2=CaCO3↓+H2O;
(2)盐酸是氯化氢的水溶液,气体的溶解度随温度的升高而减小,当加热B中溶液会闻到刺激性气味,说明溶解在水中的氯化氢由于温度升高而逸出,故填:稀盐酸;
(3)D中原来可能盛有的是氯化钠溶液,也可能是盛有的氢氧化钠溶液,氢氧化钠会与二氧化碳反应生成碳酸钠,故可以取反应后的D溶液于试管中,滴加过量的氯化钙溶液,若无白色沉淀则溶液中溶质为NaCl;若有白色沉淀.继续向上层清液中加入无色酚酞,若酚酞变红,则溶液中的溶质为NaOH和Na2CO3,若酚酞不变红,则溶液中的溶质为Na2CO3,故填:取反应后的D溶液于试管中,滴加过量的氯化钙溶液,若无白色沉淀则溶液中溶质为NaCl;若有白色沉淀.继续向上层清液中加入无色酚酞,若酚酞变红,则溶液中的溶质为NaOH和Na2CO3,若酚酞不变红,则溶液中的溶质为Na2CO3.
点评:本题考查了常见物质鉴别,完成此题,可以依据物质的性质差异进行.

练习册系列答案
相关题目