��Ŀ����
����Ŀ��ijͬѧ���������ͼ��ʾ��װ�ã�����ʵ������ȡ CO2�������IJ������ʽ���̽������Ҫ����⡣
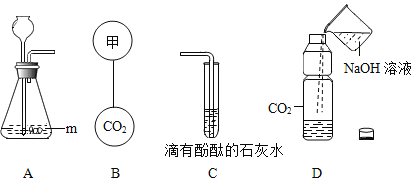
��1������ m ��������_____��A ������Ӧ�Ļ�ѧ����ʽΪ_____
��2����Ҫ B ���������������ڿ����������������_____������ţ�
A ���� B ���� C ����
��3����ͼ C �е��Թ�ͨ�� CO2��������_____������ʯ��ˮ�����ʸպ���ȫ������
��4���� D ��������ƿ��һ������ NaOH ��Һ��Ѹ��š��ƿ�棬���ɹ۲쵽ƿ�ӱ����ʹ������ƿ�ָ�ԭ״������ע������ƿע������_____�����Ա����ƣ���ַ�Ӧ���ɡ�
���𰸡���ƿ CaCO3+2HCl=CaCl2+CO2��+H2O C ��Һ��ɫ�ɺ�ɫ��Ϊ��ɫ ϡ����
��������
��1������m������Ϊ��ƿ��ʵ����������CO2���õķ�Ӧ����CaCO3��HCl������ʽΪCaCO3+2HCl=CaCl2+CO2��+H2O
��2��Ҫ�����������ڿ��м�Ҫ�����������γɵĵ���ϵƽ�⣬CO2���ܶȴ��ڿ����������ڿ����л��³�����˼�����������ܶ�С�ڿ������ۺ�����ѡ�ֻ��H2��������
��3��ʯ��ˮ������ΪCa(OH)2���Լ��ԣ���ʹ��̪��Һ��죬��CO2����Ca(OH)2��Ӧ����CaCO3��������Ca(OH)2�ܽ������ϼ��٣�����Ӧ��ȫʱ����Һ����Ca(OH)2����Һ�����ɫ����˴����Һ��ɫ�ɺ�ɫ��Ϊ��ɫ��
��4��ƿ�ӱ������ΪCO2��NaOH��Ӧ����Na2CO3����С��ƿ�ڵ�ѹǿ������ֻҪ�ܽ�CO2�ٷ�Ӧ��������������ƿ��ԭ���ܸ�Na2CO3��Ӧ����CO2�ľ��Ǽ����ϡ���ᡢϡ���ᡢϡ�������ᣬ��������һ���ɡ�
�ʴ�Ϊ��ƿ��CaCO3+2HCl=CaCl2+CO2��+H2O��C����Һ��ɫ�ɺ�ɫ��Ϊ��ɫ��ϡ����

 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�����Ŀ���ס��ҡ����������ʵ�ת����ϵ����ͼ��ʾ����������ʾ��Ӧһ��ʵ�֣��������ʺͷ�Ӧ��������ȥ��������ѡ���ʵ��ͼʾת������
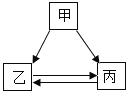
ѡ�� | �� | �� | �� |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Ca(OH)2 | CaCl2 | CaCO3 |
D | NaOH | NaCl | NaNO3 |
A. A B. B C. C D. D
����Ŀ������ʯ��ʯ����Ҫ�ɷ� CaCO3��������ʯ�ң�CaO���Ͷ�����̼��Ϊ�˲ⶨijʯ��ʯ��̼��ƣ�CaCO3���ĺ������ֳ�ȡ 24.0g ʯ��ʯ��Ʒ�������Ĵθ������ա���ȴ������ʣ���������� �����ʲ��μӷ�Ӧ������¼ʵ���������£�
���� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
ʣ��������� | 21.6g | 19.2g | 15.2g | 15.2g |
�Լ��㣺
��1����ȫ��Ӧ�����ɶ�����̼������Ϊ_____��
��2�����ʯ��ʯ��Ʒ��̼��Ƶ�����_____��