题目内容
12、A、B、C、D四种化合物,分别可能由以下两组离子中的各一种所构成:
阳离子组:Na+、Mg2+、Cu2+、Ba2+
阴离子组:OH-、Cl-、SO42-、CO32-
(1)A不溶于水,也不溶于酸
(2)B溶于水后,若与阳离子组中的另一种离子反应,有A生成;若与阴离子组中的另两种离子
反应,均产生白色浑浊现象
(3)C溶于水后,与阳离子组中的任一种离子都不反应;将一根铁棒置于C溶液中,一段时间后
铁棒增重
(4)D的水溶液显碱性,与阴离子组中的另两种离子反应,分别生成A和一种白色沉淀
请写出B、C、D的化学式:B
阳离子组:Na+、Mg2+、Cu2+、Ba2+
阴离子组:OH-、Cl-、SO42-、CO32-
(1)A不溶于水,也不溶于酸
(2)B溶于水后,若与阳离子组中的另一种离子反应,有A生成;若与阴离子组中的另两种离子
反应,均产生白色浑浊现象
(3)C溶于水后,与阳离子组中的任一种离子都不反应;将一根铁棒置于C溶液中,一段时间后
铁棒增重
(4)D的水溶液显碱性,与阴离子组中的另两种离子反应,分别生成A和一种白色沉淀
请写出B、C、D的化学式:B
MgSO4
、C
CuCl2
、D
Ba(OH)2
.分析:(1)既不溶于水又不溶于酸的沉淀包括硫酸钡和氯化银,本题中只能是硫酸钡;
(2)要生成A,B物质中必须含有硫酸根离子,同时只有镁离子会和氢氧根离子生成氢氧化镁沉淀,和碳酸根离子反应生成微溶于水的碳酸镁,故B中含有Mg2+和SO42-;
(3)阴离子组中只有Cl-与阳离子组中的任一种离子都不反应,将一根铁棒置于C溶液中,一段时间后铁棒增重,而四种阳离子中只有Cu2+会被铁置换出来,故C中含有Cu2+和Cl-;
(4)阳离子中只有钡离子既会和硫酸根离子反应生成A物质硫酸钡,又会和碳酸根离子反应生成碳酸钡白色沉淀,同时D的水溶液显碱性,所以D中含有OH-和Ba2+,
(2)要生成A,B物质中必须含有硫酸根离子,同时只有镁离子会和氢氧根离子生成氢氧化镁沉淀,和碳酸根离子反应生成微溶于水的碳酸镁,故B中含有Mg2+和SO42-;
(3)阴离子组中只有Cl-与阳离子组中的任一种离子都不反应,将一根铁棒置于C溶液中,一段时间后铁棒增重,而四种阳离子中只有Cu2+会被铁置换出来,故C中含有Cu2+和Cl-;
(4)阳离子中只有钡离子既会和硫酸根离子反应生成A物质硫酸钡,又会和碳酸根离子反应生成碳酸钡白色沉淀,同时D的水溶液显碱性,所以D中含有OH-和Ba2+,
解答:解:(1)A不溶于水,也不溶于酸,所以A是硫酸钡;
(2)B溶于水后,与阳离子组中的另一种离子反应,会生成A,所以B物质中必须含有硫酸根离子,B与阴离子组中的另两种离子反应,均会产生白色浑浊现象,那么只有镁离子会和氢氧根离子生成氢氧化镁沉淀,和碳酸根离子反应生成微溶于水的碳酸镁,根据以上分析可知B物质为硫酸镁;
(3)C溶于水后,与阳离子组中的任一种离子都不反应,所以C中含有的阳离子为Cl-,将一根铁棒置于C溶液中,一段时间后铁棒增重,由此推断出C中含有Cu2+,故C物质为氯化铜;
(4)D的水溶液显碱性,与阴离子组中的另两种离子反应,分别生成A和一种白色沉淀,所以D中含有氢氧根离子和钡离子,钡离子和硫酸根离子反应生成A物质硫酸钡,钡离子和碳酸根离子反应生成碳酸钡白色沉淀,故D为氢氧化钡.
故答案为:MgSO4;CuCl2;Ba(OH)2.
(2)B溶于水后,与阳离子组中的另一种离子反应,会生成A,所以B物质中必须含有硫酸根离子,B与阴离子组中的另两种离子反应,均会产生白色浑浊现象,那么只有镁离子会和氢氧根离子生成氢氧化镁沉淀,和碳酸根离子反应生成微溶于水的碳酸镁,根据以上分析可知B物质为硫酸镁;
(3)C溶于水后,与阳离子组中的任一种离子都不反应,所以C中含有的阳离子为Cl-,将一根铁棒置于C溶液中,一段时间后铁棒增重,由此推断出C中含有Cu2+,故C物质为氯化铜;
(4)D的水溶液显碱性,与阴离子组中的另两种离子反应,分别生成A和一种白色沉淀,所以D中含有氢氧根离子和钡离子,钡离子和硫酸根离子反应生成A物质硫酸钡,钡离子和碳酸根离子反应生成碳酸钡白色沉淀,故D为氢氧化钡.
故答案为:MgSO4;CuCl2;Ba(OH)2.
点评:本题考查酸碱盐的溶解性和离子之间的反应现象,要求我们熟悉常见的沉淀和离子之间反应的现象.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
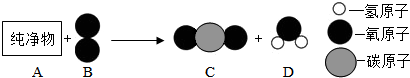
在宏观、微观和符号之间建立联系是化学学科特点.
(1)镁条在空气中燃烧时,不仅生成氧化镁和氮化镁,还有少量镁与二氧化碳反应生成碳单质和氧化镁的反应发生.
①已知氮化镁中氮元素的化合价为-3价,氮化镁的化学式为 .
②写出镁与二氧化碳反应的化学方程式 .
(2)若用 表示A元素的原子,
表示A元素的原子, 表示B元素的原子.某反应前后的物质微观示意图如下.
表示B元素的原子.某反应前后的物质微观示意图如下.
请回答下列问题.
①属于单质的物质是(填化学式,元素符号用A、B表示) .
② 和
和 中的
中的 属于同种元素,这是因为这些原子含有相同的 .
属于同种元素,这是因为这些原子含有相同的 .
③该反应前后一定不变的是 (填序号).
a.原子数目 b.元素种类 c.分子种类 d.物质总质量
(3)在一个在密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
若A与C的相对分子质量之比为15:16,则A与C的化学计量系数之比为 .
(1)镁条在空气中燃烧时,不仅生成氧化镁和氮化镁,还有少量镁与二氧化碳反应生成碳单质和氧化镁的反应发生.
①已知氮化镁中氮元素的化合价为-3价,氮化镁的化学式为 .
②写出镁与二氧化碳反应的化学方程式 .
(2)若用
 表示A元素的原子,
表示A元素的原子, 表示B元素的原子.某反应前后的物质微观示意图如下.
表示B元素的原子.某反应前后的物质微观示意图如下.
请回答下列问题.
①属于单质的物质是(填化学式,元素符号用A、B表示) .
②
 和
和 中的
中的 属于同种元素,这是因为这些原子含有相同的 .
属于同种元素,这是因为这些原子含有相同的 .③该反应前后一定不变的是 (填序号).
a.原子数目 b.元素种类 c.分子种类 d.物质总质量
(3)在一个在密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
| 物质 | A | B | C | D |
| 反应前质量 (g) | 20 | 2 | 22 | 1 |
| 反应后质量(g) | x | 2 | 14 | 24 |
 表示A元素的原子,
表示A元素的原子, 表示B元素的原子.某反应前后的物质微观示意图如下.
表示B元素的原子.某反应前后的物质微观示意图如下.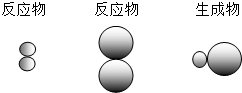
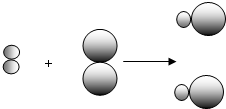 和
和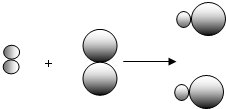 中的
中的 属于同种元素,这是因为这些原子含有相同的
属于同种元素,这是因为这些原子含有相同的