题目内容
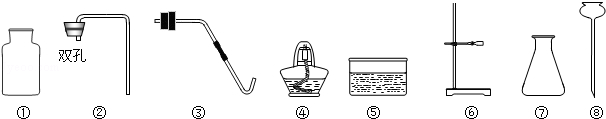
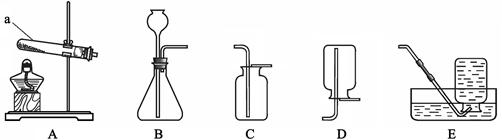
(6分)实验室制取气体所需的装置如下图所示,请回答以下问题。

(1)实验仪器a的名称是________。
(2)用过氧化氢溶液和二氧化锰制取氧气的化学方程式为________。用高锰酸钾制取氧气时,所选用的发生装置为________(填字母序号,下同)。
(3)用大理石和稀盐酸制取二氧化碳的化学方程式为________。用装置________收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到________,说明瓶中已充满二氧化碳。

(1)实验仪器a的名称是________。
(2)用过氧化氢溶液和二氧化锰制取氧气的化学方程式为________。用高锰酸钾制取氧气时,所选用的发生装置为________(填字母序号,下同)。
(3)用大理石和稀盐酸制取二氧化碳的化学方程式为________。用装置________收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到________,说明瓶中已充满二氧化碳。
(1)铁架台
(2)2H2O2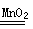 2H2O+ O2↑;B
2H2O+ O2↑;B
(3)CaCO3+2HCl=CaCl2+ H2O+CO2↑;D ;火焰熄灭
(2)2H2O2
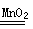 2H2O+ O2↑;B
2H2O+ O2↑;B(3)CaCO3+2HCl=CaCl2+ H2O+CO2↑;D ;火焰熄灭
试题分析:(1)实验仪器a的名称是铁架台。
(2)用过氧化氢溶液和二氧化锰制取氧气的化学方程式为:2H2O2
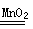 2H2O+ O2↑。用高锰酸钾制取氧气时,应选用固体在加热的情况下制取气体的反应装置,即选用装置B。
2H2O+ O2↑。用高锰酸钾制取氧气时,应选用固体在加热的情况下制取气体的反应装置,即选用装置B。(3)用大理石和稀盐酸制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+ H2O+CO2↑。因为CO2能溶于水,不能用排水法收集;CO2的密度比空气大,可用向上排空气法收集。所以可选用装置D收集。二氧化碳不支持燃烧,可把燃着的木条放在集气瓶口,若火焰熄灭,证明瓶内已充满CO2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目