题目内容
根据二氧化碳的化学式计算:
(1)二氧化碳的相对分子质量;
(2)二氧化碳中各元素的质量比;
(3)二氧化碳中碳元素的质量分数(精确到0.1%);
(4)22克二氧化碳中含有碳多少克?
(1)二氧化碳的相对分子质量;
(2)二氧化碳中各元素的质量比;
(3)二氧化碳中碳元素的质量分数(精确到0.1%);
(4)22克二氧化碳中含有碳多少克?
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据物质中某元素的质量分数的计算方法来分析.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据物质中某元素的质量分数的计算方法来分析.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)二氧化碳的相对分子质量为12+16×2=44.
(2)二氧化碳里碳元素和氧元素的质量比是12:(16×2)=3:8.
(3)二氧化碳含有碳元素的质量分数是:
×100%≈27.3%.
(4)22克里二氧化碳含有碳元素的质量为22g×
×100%=6g.
故答案为:(1)44;(2)3:8;(3)27.3%;(4)6g.
(2)二氧化碳里碳元素和氧元素的质量比是12:(16×2)=3:8.
(3)二氧化碳含有碳元素的质量分数是:
| 12 |
| 12+16×2 |
(4)22克里二氧化碳含有碳元素的质量为22g×
| 12 |
| 44 |
故答案为:(1)44;(2)3:8;(3)27.3%;(4)6g.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
如图是甲、乙两种固体物质的溶解度曲线,下列说法中正确的是( )
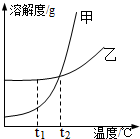

| A、将等质量的甲、乙的饱和溶液分别由t2℃降温至t1℃,析出甲多 |
| B、t2℃时,甲、乙两溶液中溶质的质量分数相等 |
| C、将甲溶液从t2℃降温到t1℃时,一定有晶体析出 |
| D、将t2℃时乙的饱和溶液变为不饱和溶液,可采取降温的方法 |
下列各物质的名称或俗称与其化学式不一致的是( )
| A、生石灰 氧化钙CaO |
| B、烧碱 纯碱 NaOH |
| C、金刚石 石墨 C |
| D、硫酸铜晶体 胆矾 CuSO4?5H2O |
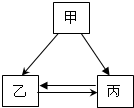 下列各组物质间通过一步反应就能实现如图转化,则甲、乙、丙可能的组合是( )
下列各组物质间通过一步反应就能实现如图转化,则甲、乙、丙可能的组合是( )| A、C CO2 CO |
| B、CuO CuCl2 Cu(OH)2 |
| C、NaOH NaCl NaNO3 |
| D、H2O H2O2 O2 |
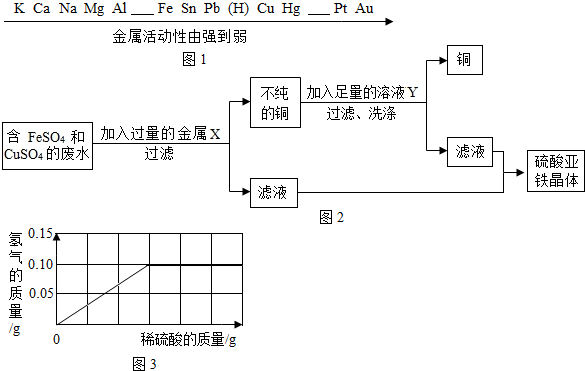
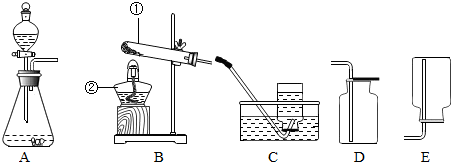
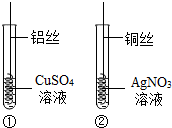 小亮为探究Cu、Al、Ag的金属活动性顺序,做了以下两个实验.请分析实验,完成填空.
小亮为探究Cu、Al、Ag的金属活动性顺序,做了以下两个实验.请分析实验,完成填空.