题目内容
 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用的试剂可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用的试剂可能是( )| 甲 | 乙 | |
| A | 双氧水和MnO2 | NaOH溶液和CO2 |
| B | 稀硫酸和铜片 | 水和CO2 |
| C | Na2CO3溶液和稀硫酸 | NaOH溶液和SO2 |
| D | H2O和NH3 | 硝酸银溶液和HCl |
| A、A | B、B | C、C | D、D |
考点:反应现象和本质的联系,实验室制取氧气的反应原理,酸的化学性质,碱的化学性质,盐的化学性质
专题:结合课本知识的信息
分析:根据容器内气体压强与外界大气的压强相对大小判断.
解答:解:A、甲中双氧水在二氧化锰的催化下迅速反应生成氧气,使容器内压强大于大气压,所以气球变大;乙中二氧化碳极易溶于氢氧化钠溶液,导致容器内的压强小于大气压,所以气球变大,故正确.
B、甲中稀硫酸和铜片不反应,所以容器内气体压强不变,气球不变化;乙中二氧化碳部分溶于水,使容器内的压强小于大气压,所以气球变大,故错误.
C、甲中稀硫酸和碳酸钠反应生成二氧化碳,导致容器内压强大于大气压,所以气球变大;乙中二氧化硫极易溶于氢氧化钠溶液,导致容器内的压强小于大气压,所以气球变大,故正确.
D、甲中氨气极易溶于水,导致容器内压强小于大气压,所以气球不会胀大;乙中硝酸银和HCl反应生成白色沉淀,导致容器内压强小于大气压,所以气球变大,故错误.
故选AC.
B、甲中稀硫酸和铜片不反应,所以容器内气体压强不变,气球不变化;乙中二氧化碳部分溶于水,使容器内的压强小于大气压,所以气球变大,故错误.
C、甲中稀硫酸和碳酸钠反应生成二氧化碳,导致容器内压强大于大气压,所以气球变大;乙中二氧化硫极易溶于氢氧化钠溶液,导致容器内的压强小于大气压,所以气球变大,故正确.
D、甲中氨气极易溶于水,导致容器内压强小于大气压,所以气球不会胀大;乙中硝酸银和HCl反应生成白色沉淀,导致容器内压强小于大气压,所以气球变大,故错误.
故选AC.
点评:本题考查了常见气体的制备原理及装置选择,同时考查酸、碱、盐的性质,要理解和掌握酸、碱、盐常见的化学反应.

练习册系列答案
相关题目
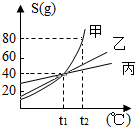 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是( )
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是( )| A、t2℃时丙物质的溶解度最小 |
| B、甲物质的溶解度受温度的影响最大 |
| C、要使t1℃时甲物质的饱和溶液变成不饱和溶液,可以采取升高温度的方法 |
| D、t2℃时,往100g水中加入90g乙物质,充分搅拌后得到190g乙物质的溶液 |
在一定条件下,下列物质间的转化一步不能实现的是( )
| A、Fe→Fe3O4 |
| B、Fe2O3→Fe |
| C、S→SO3 |
| D、NaOH→Na2SO4 |
“水是人类必不可少的宝贵资源,没有水就没有生命”.下列关于水的说法错误的是( )
| A、水在自然界中不断循环,淡水取之不尽、用之不竭 |
| B、水能溶解很多物质,在生物体内起着运送营养物质的作用 |
| C、加强工业废水的排放监控,生活废水应坚持达标排放和集中排放 |
| D、水在自然界中以固态、液态、气态形式存在,水对调节地球温度起到了重要的作用 |
如图是元素周期表中的四种元素及相关粒子的结构示意图,请你判断选项中哪种物质是由所提供的粒子构成的( )


| A、MgCl2 |
| B、Na2S |
| C、NaCl |
| D、Mg |
类推是学习化学的一种重要方法,以下类推正确的是( )
| A、碱能跟非金属氧化物反应,则碱溶液一定能吸收CO2、SO2和CO |
| B、物质都由元素组成,同种元素可组成纯净物,则不同种元素也可组成纯净物 |
| C、分解反应能生成两种或两种以上其他物质,则生成两种或两种以上其他物质的反应一定是分解反应 |
| D、钠原子核外最外电子层上排布着一个电子,属于金属元素的原子,则最外电子层上排布着一个电子的原子一定是金属元素的原子 |
对下列叙述的微观解释中,不正确的是( )
| A、槐花飘香:分子不停的运动 |
| B、水烧开后易把壶盖顶起:温度升高,分子变大 |
| C、CO和CO2的化学性质不同:二者的分子构成不同 |
| D、化学反应遵守质量守恒定律:化学反应前后原子的种类、数目、质量没有改变 |
下列图示中实验基本操作错误的是( )
A、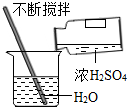 稀释浓硫酸 |
B、 检查气密性 |
C、 液体加热 |
D、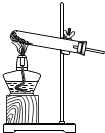 固体加热 |