题目内容
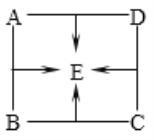
【题目】如图是A、B、C三种物质的溶解度曲线,据图回答:

(1)M点表示的意义是________________;
(2)t1℃时30gA物质加入到50g水中不断搅拌,充分溶解形成的溶液质量是_______。
(3)将t1℃时三种物质的饱和溶液升温至t2℃时,所得溶液溶质的质量分数大小关系是_______。
【答案】 t2℃时,A、B两物质的溶解度相等 65g B>C>A
【解析】(1)M点表示的意义是t2℃时,A、B两物质的溶解度相等。(2)t1℃时,A的溶解度是30g,则50g水中最多溶解15gA,故30gA物质加入到50g水中,充分溶解形成的溶液质量是50g+15g=65g。(3)将t1℃时三种物质的饱和溶液升温至t2℃时,C的溶解度减小,溶质质量分数变小,A、B的溶解度增大,变为不饱和溶液,溶质质量分数不变,故所得溶液溶质的质量分数大小关系是B>C>A。

【题目】某研究性学习小组对炭粉与氧化铜反应产物中气体的成分进行研究。
【提出假设】该反应的气体产物中有二氧化碳和其他气体。
【查阅资料】氮气不能跟炭粉和氧化铜发生反应,也不跟石灰水反应,可用来隔绝氧气。
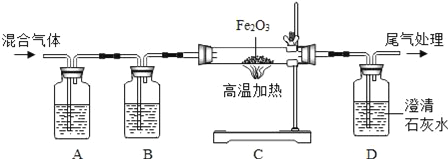
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量炭粉充分反应。通过测定反应前后相关物质的质量进行判断。
【进行实验】

操作步骤 | 实验现象及分析 |
取1.6 g氧化铜与1 g炭粉均匀混合,放入质量为48.2 g的B装置的玻璃管中。 | |
打开弹簧夹,往贮气瓶A中注入水,将氮气通入B装置中。 | ①水应从_______端注入(填“a”或“b”)。 |
先通一段时间氮气。 | ②目的是_____________。 |
夹紧弹簧夹,用酒精喷灯加热玻璃管内的混合物。 | ③玻璃管中的现象是______________。 |
停止加热,再通入一段时间氮气。 | ④目的是________________。 |
实验完毕后,冷却装置至室温,称得B玻璃管及固体总质量为50.2 g,称得C瓶中液体增重0.4 g。 | ⑤结论:原假设_____(填“成立”或“不成立”),理由是____________(用计算式表示)。 |