题目内容
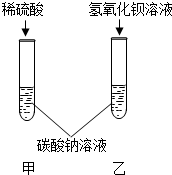 甲乙两同学为了验证碳酸钠的化学性质,做了如图所示的实验.乙同学的实验中发生反应的化学方程式为
甲乙两同学为了验证碳酸钠的化学性质,做了如图所示的实验.乙同学的实验中发生反应的化学方程式为Na2CO3+Ba(OH)2═BaCO3↓+2NaOH
Na2CO3+Ba(OH)2═BaCO3↓+2NaOH
.试验后,乙同学将除去沉淀后的废液倒入烧杯中,然后甲同学也将废液缓慢倒入同一烧杯中,发现烧杯中开始时没有现象,随后产生气泡.
根据上述现象推断,甲,乙两同学试管中的废液所含溶质分别是:甲
Na2SO4、H2SO4
Na2SO4、H2SO4
乙NaOH、Na2CO3
NaOH、Na2CO3
(均写化学式)【提出问题】:最终烧杯中的废液含有的溶质是多少
【猜想与假设】
猜想①:废液中含有Na2SO4 H2SO4两种物质.
猜想②:废液中只含有Na2SO4一种物质.
【活动与探究】
甲、乙同学为了验证猜想,分别取少量烧杯中的废液于试管中,进行了如下实验.
| 实验方案 | 现象 | 结论 | |
| 甲同学 | 向试管中滴加石蕊溶液 | 溶液变红 溶液变红 |
猜想①正确 |
| 乙同学 | 向试管中滴加稀盐酸 | 无明显现象 | 猜想①正确 |
硫酸钠不能和稀盐酸反应,若溶液中只有硫酸钠,溶液中也没有明显的现象
硫酸钠不能和稀盐酸反应,若溶液中只有硫酸钠,溶液中也没有明显的现象
.分析:碳酸钠可以和氢氧化钡溶液反应生成碳酸钡沉淀和氢氧化钠,可以据此写出反应的化学方程式;
将甲中的废液倒入乙中,开始没有气体产生说明在溶液中含有氢氧化钠,所以可以判断在乙中含有的溶质为氢氧化钠和碳酸钠,而在甲中含有的溶质为硫酸钠和硫酸,可以据此解答该题;
【活动与探究】石蕊遇酸变红,可以据此解答;
【反思与评价】硫酸钠不能和稀盐酸反应,可以据此解答该题.
将甲中的废液倒入乙中,开始没有气体产生说明在溶液中含有氢氧化钠,所以可以判断在乙中含有的溶质为氢氧化钠和碳酸钠,而在甲中含有的溶质为硫酸钠和硫酸,可以据此解答该题;
【活动与探究】石蕊遇酸变红,可以据此解答;
【反思与评价】硫酸钠不能和稀盐酸反应,可以据此解答该题.
解答:解:碳酸钠可以和氢氧化钡溶液反应生成碳酸钡沉淀和氢氧化钠,该反应的化学方程式为:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH;
将甲中的废液倒入乙中,开始没有气体产生说明在溶液中含有氢氧化钠,所以可以判断在乙中含有的溶质为氢氧化钠和碳酸钠,其化学式为:NaOH、Na2CO3;而在甲中含有的溶质为硫酸钠和硫酸,其化学式为:Na2SO4、H2SO4;
【活动与探究】石蕊遇酸变红,所以根据甲同学的实验结论可以判断实验现象为溶液变红;
【反思与评价】硫酸钠不能和稀盐酸反应,若溶液中只有硫酸钠,溶液中也没有明显的现象,故乙同学的结论错误.
故答案为:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH;
Na2SO4、H2SO4;NaOH、Na2CO3;
【活动与探究】溶液变红;
【反思与评价】硫酸钠不能和稀盐酸反应,若溶液中只有硫酸钠,溶液中也没有明显的现象.
将甲中的废液倒入乙中,开始没有气体产生说明在溶液中含有氢氧化钠,所以可以判断在乙中含有的溶质为氢氧化钠和碳酸钠,其化学式为:NaOH、Na2CO3;而在甲中含有的溶质为硫酸钠和硫酸,其化学式为:Na2SO4、H2SO4;
【活动与探究】石蕊遇酸变红,所以根据甲同学的实验结论可以判断实验现象为溶液变红;
【反思与评价】硫酸钠不能和稀盐酸反应,若溶液中只有硫酸钠,溶液中也没有明显的现象,故乙同学的结论错误.
故答案为:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH;
Na2SO4、H2SO4;NaOH、Na2CO3;
【活动与探究】溶液变红;
【反思与评价】硫酸钠不能和稀盐酸反应,若溶液中只有硫酸钠,溶液中也没有明显的现象.
点评:本题属于实验探究题,还有化学方程式的书写,综合性比较强.有关实验方案的设计是中考的热点之一,本题根据题目提供的信息,结合实验探究的一般步骤和酸碱盐的性质等知识来解决,还要注意化学方程式的书写和配平.本考点主要出现在实验题中.

练习册系列答案
相关题目

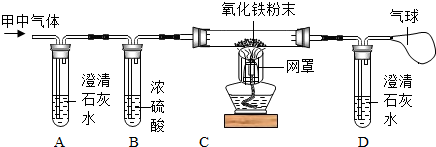
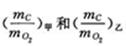 。 当小明和小芳的猜想均成立时,则
。 当小明和小芳的猜想均成立时,则 (填>”、“<”或=”)
(填>”、“<”或=”)