题目内容
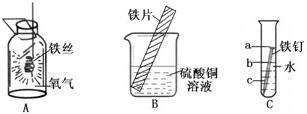
金属的化学性质:常见的金属有铜、铁、铝(写出它们下列反应的化学方程式)(1)在加热或点燃的条件下,它们与O2能反应:
(2)与稀硫酸的反应:
(3)与盐酸的反应:
(4)与硫酸铜溶液的反应:
以上(2)-(4)反应中反应的基本类型是
分析:(1)金属可以与氧气发生反应,反应生成金属氧化物;
(2)(3)与酸反应会生成氢气并发生置换反应;
(4)活泼的金属能把活动性弱的金属从其盐溶液中置换出来.
置换反应的特点是:单质与化合物生成单质与化合物
(2)(3)与酸反应会生成氢气并发生置换反应;
(4)活泼的金属能把活动性弱的金属从其盐溶液中置换出来.
置换反应的特点是:单质与化合物生成单质与化合物
解答:解:由题意知:反应物、生成物,根据质量守恒定律,正确书写化学方程式;如铁与盐酸反应:反应物为铁与盐酸,生成物为氯化亚铁与氢气,根据质量守恒定律,故正确书写化学方程式 Fe+2HCl=FeCl2+H2↑;同理,可知其他反应的反应物和生成物,以及各化学方程式的书写.
故答案为:(1)2Cu+O2
2CuO;2Al+302
2Al203;3Fe+2O2
Fe3O4
(2)Fe+H2SO4=FeSO4+H2↑; 2Al+3H2SO4=Al2(SO4)3+3H2↑.
(3)Fe+2HCl=FeCl2+H2↑; 2Al+6HCl=2AlCl3+3H2↑
(4)Fe+CuSO4═FeSO4+Cu;2Al+3CuSO4═Al2(SO4)3+3Cu.
置换反应,单质与化合物生成单质与化合物.
故答案为:(1)2Cu+O2
| ||
| ||
| ||
(2)Fe+H2SO4=FeSO4+H2↑; 2Al+3H2SO4=Al2(SO4)3+3H2↑.
(3)Fe+2HCl=FeCl2+H2↑; 2Al+6HCl=2AlCl3+3H2↑
(4)Fe+CuSO4═FeSO4+Cu;2Al+3CuSO4═Al2(SO4)3+3Cu.
置换反应,单质与化合物生成单质与化合物.
点评:根据题目信息,找出反应物和生成物,再利用书写化学方程式的方法及步骤,根据质量守恒定律,正确书写化学方程式;掌握金属的化学性质和置换反应的概念及其应用

练习册系列答案
相关题目