题目内容
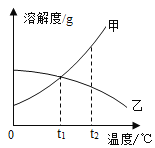
【题目】甲、乙两种物质的溶解度曲线如下图所示。t1℃时,将等质量的水分别加入到各盛有等质量甲、乙的试管中,充分振荡后,试管底部均有未溶解的固体,再将其温度都升高到t2℃。
0
(1)t1℃时,等质量甲、乙分别配成饱和溶液,所需水的质量甲____乙(填“>”“<”或“=”);
(2)若不考虑水分的蒸发,由t1℃升温到t2℃的过程中,下列说法正确的是_____(填序号,下同);
A 甲乙两种物质的溶解度都增大 B 甲物质的溶解度小于乙物质的溶解度
C 甲溶液的质量减小 D 装有乙物质的试管中剩余固体增多
(3)通常情况下,在实验室用甲和水配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平、烧杯和___。
A 酒精灯 B 药匙 C 玻璃棒 D 漏斗 E 铁架台 F 量筒 G 胶头滴管
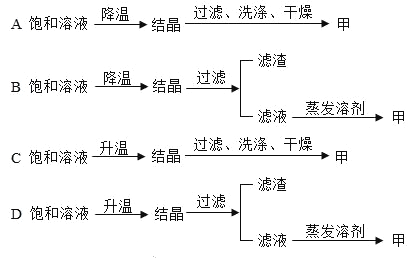
(4)现有t2℃甲的饱和溶液,其中含少量乙。为得到纯净的甲物质,下列设计方案正确的是__。
【答案】= D BCFG A
【解析】
(1)t1℃时,甲和乙的溶解度相等,等质量甲、乙分别配成饱和溶液,所需水的质量相等;故填:=。
(2)t1℃时,将等质量的水分别加入到各盛有等质量甲、乙的试管中,充分振荡后,试管底部均有未溶解的固体,说明均为饱和溶液,再将其温度都升高到t2℃;
A、甲物质的溶解度都增大,乙减小,故错误;
B、甲物质的溶解度大于乙物质的溶解度,故错误;
C、甲溶液的质量增大,故错误;
D、装有乙物质的试管中剩余固体增多,故正确;故选D。
(3)用固体配制一定质量分数的溶液需用到的仪器有:托盘天平、烧杯和药匙、玻璃棒、量筒、胶头滴管,故选BCFG。
(4)现有t2℃甲的饱和溶液,其中含少量乙。为得到纯净的甲物质,甲的溶解度随温度升高而增大,应该降温结晶获得甲,经过滤、洗涤干燥,可得到纯净的甲物质,故选A。

【题目】在一密闭容器内加入甲、乙、丙、丁四种物质,测得反应前后各物质的质量如下表所示:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
下列说法错误的是( )
A.x等于0
B.该反应可能为置换反应
C.该反应中甲与乙质量的变化比为48: 23
D.该反应遵循质量守恒定律
【题目】石灰石高温煅烧获得的生石灰是炼钢生产中的主要碱性造渣材料,其活性度好坏对冶炼过程有重要影响。
(提出问题)哪些因素可能影响生石灰的活性度?
(查阅资料)生石灰活性度体现了生石灰与其他物质的反应能力,是表征生石灰水化反应速度的一个指标。生产中常用的检测标准定义为:在足够时间内,用中和生石灰消化时产生的Ca(OH)2所消耗的盐酸的体积数(单位为mL)表示。
(进行实验)
实验1:相同条件下,煅烧不同石灰石,测生石灰的活性度。
产地 | 石灰石 | 生石灰 | |
外观 | CaO含量/% | 活性度/mL | |
A地 | 灰白色 | 94.89 | 391 |
B地 | 灰白色带少量红棕色 | 89.97 | 375 |
实验2:取某石灰石试样,在电炉内进行煅烧,烧成后测定生石灰的活性度。
时间/min | 各煅烧温度下的生石灰活性度/mL | |||||
1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ | |
12 | 790 | 836 | 868 | 808 | 454 | 412 |
16 | 793 | 856 | 871 | 845 | 556 | 530 |
20 | 795 | 863 | 873 | 864 | 617 | 623 |
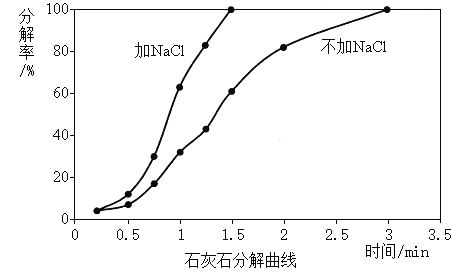
实验3:煅烧温度1050℃时,加NaCl和不加NaCl,比较煅烧石灰石的分解率(分解率影响生石灰活性度)。
(解释与结论)
(1)实验1的目的是___________。
(2)能证明最佳煅烧温度为1100~1200℃的证据是__________。
(3)实验3的结论是_________。
(反思与评价)
(4)写出石灰石高温分解生成生石灰和另一种氧化物的化学方程式_________。
(5)除以上研究的可能影响生石灰活性度的因素外,你认为还可以研究的其他因素有_______(写出一条即可)。