题目内容
【题目】二氧化碳是导致温室效应的主要气体,也是一种宝贵的资源,用CO2和NH3来合成尿素[CO(NH2)2]是固定和利用CO2的成功范例,其反应的化学方程式为:
CO2+2NH3![]() CO(NH2)2+H2O
CO(NH2)2+H2O
请计算下列问题:
(1)若利用CO2和NH3生产900t尿素,理论上可固定CO2的质量是多少吨?
(2)2t含尿素90%的化肥(杂质不含N)中,含氮元素的质量是多少吨?(精确到0.1t).
【答案】 (1)660t;(2)0.84t
【解析】
试题分析:(1)设生产1000万吨尿素需要二氧化碳的质量为x,
CO2+2NH3![]() CO(NH2)2+H2O
CO(NH2)2+H2O
44 60
x 900t
![]()
x=660t
(2)经测定某尿素样品含尿素90%,2t该样品中尿素的质量为2×90%=1.8t
其中含氮元素的质量为1.8t××![]() =0.84t
=0.84t
答:(1)理论上可固定CO2的质量是660t[来源:](2)含氮元素的质量是0.84t

练习册系列答案
相关题目
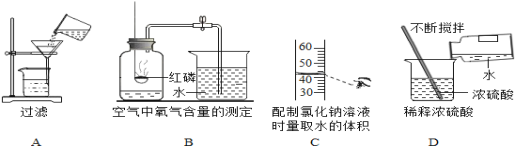
【题目】除去下列物质中的少量杂质,所选用的试剂及操作方法不正确的是( )
选项 | 物质 | 杂质 | 试剂及操作方法 |
A | CuO粉末 | Cu粉 | 加适量稀盐酸、过滤 |
B | CaCO3 | CaO | 加足量水、充分反应后过滤 |
C | N2气体 | O2气体 | 通过灼热的铜网 |
D | NaCl溶液 | Na2CO3溶液 | 加入适量的稀盐酸 |
A.A B.B C.C D.D