题目内容
氢气的燃烧值为1.4×108焦/千克,燃烧产物不污染环境,是一种未来能源.我国于1980年成功地研制出国内第一辆以氢气为动力的汽车.燃氢汽车发动机中发生反应的化学方程式为:________;若这种汽车行驶1小时需1.68×108焦的热量,则每小时需要消耗氢气________千克(不计热量损失).
2H2+O2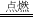 2H2O 1.2
2H2O 1.2
分析:根据氢气燃烧生成水写出反应的化学方程式,然后根据“汽车行驶1h需要的热量÷氢气的热值=每小时需要消耗氢气的质量”计算即可.
解答:氢气燃烧生成物为水,燃氢汽车发动机中发生反应的化学方程式为2H2+O2 2H2O;每小时需要消耗氢气的质量=1.68×108J÷1.4×108J/kg=1.2kg.
2H2O;每小时需要消耗氢气的质量=1.68×108J÷1.4×108J/kg=1.2kg.
故答案为:2H2+O2 2H2O;1.2.
2H2O;1.2.
点评:本题主要考查学生的化学方程式的书写以及计算能力.要知道物质发生化学变化时的能量变化情况,能够在生活中正确的利用好放出的热量或吸收热量.
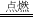 2H2O 1.2
2H2O 1.2分析:根据氢气燃烧生成水写出反应的化学方程式,然后根据“汽车行驶1h需要的热量÷氢气的热值=每小时需要消耗氢气的质量”计算即可.
解答:氢气燃烧生成物为水,燃氢汽车发动机中发生反应的化学方程式为2H2+O2
 2H2O;每小时需要消耗氢气的质量=1.68×108J÷1.4×108J/kg=1.2kg.
2H2O;每小时需要消耗氢气的质量=1.68×108J÷1.4×108J/kg=1.2kg.故答案为:2H2+O2
 2H2O;1.2.
2H2O;1.2.点评:本题主要考查学生的化学方程式的书写以及计算能力.要知道物质发生化学变化时的能量变化情况,能够在生活中正确的利用好放出的热量或吸收热量.

练习册系列答案
相关题目