题目内容
【题目】某兴趣小组为了验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式 .
(2)小霖发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我(填“同意”或“不同意”)小霖的观点,因为 .
(3)小明同学按如图所示的装置改进实验,验证了质量守恒定律,却发现产物中还有少量淡黄色固体.
[提出问题]淡黄色固体是什么?
物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
[查阅资料]小明同学查阅资料,记录了下列几种含有镁元素的物质的颜色.
其他同学认为不必查阅氯化镁的颜色,理由是;
[提出猜想]分析资料,根据颜色判断,李霖认为该淡黄色固体应该是 , 可能是由镁与空气中的反应生成的,反应的化学方程式为 .
[实验探究]小霖设计实验证实了自己的猜想,她的方案可能;
[反思与评价]通过上述实验,我们可以发现燃烧不一定需要氧气.
[相关结论]空气中氮气(N2)和氧气(O2)的体积比约为 , 但镁条在空气中燃烧只生成少量的淡黄色固体,由此得出的一个结论是 . 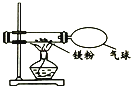
【答案】
(1)2Mg+O2![]() 2MgO
2MgO
(2)不同意;所有的化学反应都遵循质量守恒定律
(3)空气的成分中不含氯元素;氮化镁;氮气(或N2);3Mg+N2![]() Mg3N2;将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;4:1;氮气含量多但是很稳定,难以发生反应
Mg3N2;将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;4:1;氮气含量多但是很稳定,难以发生反应
【解析】(1)在点燃的条件下,镁与氧气反应生成氧化镁,化学方程式为:2Mg+O2![]() 2MgO;(2)所有的化学变化都遵循质量守恒定律;(3)[查阅资料]根据质量守恒定律,化学反应前后元素的种类不变,由于空气中无氯元素,所以燃烧产物中一定不存在氯化镁; [提出猜想]空气中含有氮气,在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体,而氮化镁为淡黄色,所以淡黄色的固体可能是镁与空气中的氮气反应生成的.镁和氮气在点燃的条件下反应生成氮化镁,化学方程式:3Mg+N2
2MgO;(2)所有的化学变化都遵循质量守恒定律;(3)[查阅资料]根据质量守恒定律,化学反应前后元素的种类不变,由于空气中无氯元素,所以燃烧产物中一定不存在氯化镁; [提出猜想]空气中含有氮气,在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体,而氮化镁为淡黄色,所以淡黄色的固体可能是镁与空气中的氮气反应生成的.镁和氮气在点燃的条件下反应生成氮化镁,化学方程式:3Mg+N2![]() Mg3N2 . [实验探究]由于在纯氧气中燃烧镁条只生成白色固体氧化镁,在纯氮气中燃烧镁条只生成淡黄色色固体氮化镁,可用在纯氮气中燃烧镁条,观察现象的方法. [相关结论]空气中氮气(N2)和氧气(O2)的体积比约为4:1,但镁条在空气中燃烧只生成少量的淡黄色固体,由此得出的一个结论是氮气含量多但是很稳定,难以发生反应.
Mg3N2 . [实验探究]由于在纯氧气中燃烧镁条只生成白色固体氧化镁,在纯氮气中燃烧镁条只生成淡黄色色固体氮化镁,可用在纯氮气中燃烧镁条,观察现象的方法. [相关结论]空气中氮气(N2)和氧气(O2)的体积比约为4:1,但镁条在空气中燃烧只生成少量的淡黄色固体,由此得出的一个结论是氮气含量多但是很稳定,难以发生反应.
【考点精析】通过灵活运用书写化学方程式、文字表达式、电离方程式,掌握注意:a、配平 b、条件 c、箭号即可以解答此题.

 备战中考寒假系列答案
备战中考寒假系列答案