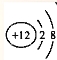题目内容
【题目】化学以实验为基础,学好化学要做好实验。
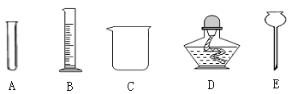
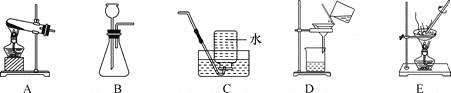
(1)实验前要熟悉实验仪器及基本操作。如图是初中化学实验室常用的五种仪器,其中既可以作为反应容器,又可以在加热时使用的是__________(填序号),仪器E的名称是___________。
(2)化学实验要严格按操作要求进行,在横线上填写以下错误操作造成的后果:
①实验室用剩的药品放回原瓶_______________;
②用量筒量取20mL水仰视读数,量取水的体积会_____(填“偏大”或“偏小”)。
(3)实验时要认真观察实验现象,学会分析得出正确结论。能从如图所示实验及现象得出的结论有___________(填序号)。

A.二氧化碳密度比空气大 B.二氧化碳不能燃烧
C.二氧化碳不支持燃烧 D.蜡烛燃烧产物中含有二氧化碳
【答案】A 长颈漏斗 污染了药品 偏大 ABC
【解析】
(1)根据常用仪器的名称和用途分析回答;
(2)①根据剩余药品的处理方法解答,做的“三不一要”,即不能放回原瓶,也不要随意丢弃,更不要拿出实验室,应该要放入指定容器;
②量取液体时,仰视量筒的刻度,会使读数偏小,实际量得液体体积偏大;
(3)根据实验的现象分析二氧化碳的性质。
(1)由图示可知,既可以作为反应容器,又可以在加热时使用的是试管,仪器E的名称是长颈漏斗;
(2)①实验室用剩的药品放回原瓶污染了药品;
②用量筒量取20mL水仰视读数,量取水的体积会偏大;
(3)由实验的现象是:下面的蜡烛先熄灭,上面的蜡烛后熄灭,可得出二氧化碳的性质是:二氧化碳密度比空气大、不能燃烧,也不支持燃烧。

练习册系列答案
相关题目