题目内容
【题目】某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费。初三(2)班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理。
(1)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:

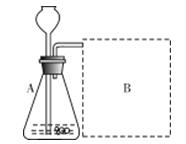
①废水在加入金属X前需进行过滤,目的是将其中__________性杂质除去。进行过滤的操作所需的仪器有:________、________、________、________(请从下图中选择合适仪器,并用仪器名称填写)。

②金属X是_____________,其加入废水后发生反应的化学方程式为___ ____溶液Y是________利用其除去铜中杂质,有关反应的化学方程式为______________
【答案】①不溶 烧杯、玻璃棒、铁架台、漏斗
②Fe(或铁) Fe+CuSO4===FeSO4+Cu 稀硫酸 Fe+H2SO4===FeSO4+H2↑
【解析】
试题分析:①过滤就是将不溶性固体与液体分离,故废水在加入金属X前需进行过滤,目的是将其中不溶性杂质除去。进行过滤的操作所需的仪器有:烧杯、玻璃棒、铁架台、漏斗
②因为最终得到的是纯净的硫酸亚铁晶体,故金属X是Fe(或铁);加入废水后发生反应的化学方程式为: Fe+CuSO4===FeSO4+Cu;由于所加的铁是过量的,故不纯的铜中还有过量的铁,为了将铁除去,同时还得到硫酸亚铁,故溶液Y是稀硫酸;发生反应的化学方程式为:Fe+H2SO4===FeSO4+H2↑

练习册系列答案
相关题目