题目内容
【题目】如图是几种初中化学常见物质的转化关系的示意图(部分产物未标出),其中A、D均属于碳酸盐。回答下列问题:
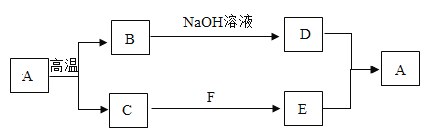
(1)写出下列物质的化学式:C_______,D____。
(2)写出D与E反应的化学方程式:_____。
【答案】![]()
![]()
![]()
【解析】
由题意A是碳酸盐,高温能分解为B和C,推测A为碳酸钙,碳酸钙高温条件分解为氧化钙和二氧化碳,则B和C可能为氧化钙或二氧化碳,B能与氢氧化钠溶液反应,推测B为二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠和水,D为碳酸钠,属于碳酸盐,推测C为氧化钙,F为水,氧化钙与水反应生成E氢氧化钙,D与E的反应即氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠。经过验证,以上物质的推测合理,则有:
(1) C为氧化钙,化学式为![]() ;D为碳酸钠,化学式为
;D为碳酸钠,化学式为![]() 。
。
(2)根据推断,D为碳酸钠,E为氢氧化钙,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为![]() 。
。

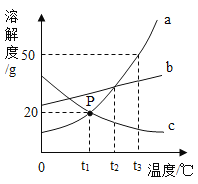
【题目】25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是
编号 | ① | ② | ③ | ④ |
水的质量/g | 50 | 50 | 50 | 50 |
加入固体质量/g | 5 | 10 | 15 | 20 |
现象 | 固体完全溶解 | 固体完全溶解 | 剩余少量固体 | 剩余较多固体 |
A.实验①所得溶液的溶质质量分数是实验②的一半
B.在实验④中再加入 50g水后,溶液的溶质质量分数为 15%
C.由表格中的数据可以确定 25℃时该物质的溶解度大小的范围是:20 g≤S<30g
D.实验②中温度由 25℃冷却到 10℃时,一定有固体析出
【题目】碳酸锂是一种重要的锂盐,广泛应用于锂离子电池生产中。工业上可以用锂辉石精矿(主要成分是Li2O、含有Al2O3、SiO2等杂质) 为原料制取高纯的碳酸锂。某校化学活动小组收集了碳酸锂的溶解度数据如表:
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度(g) | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
设计了制取碳酸锂的工艺流程(如图):
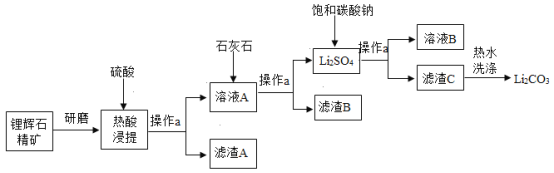
请回答:
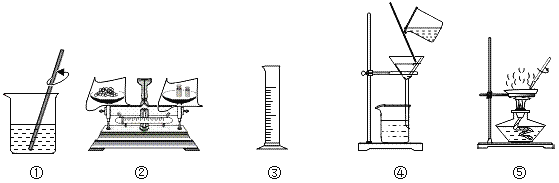
(1)操作a所需的玻璃仪器有烧杯、玻璃棒和_____。
(2)热酸浸提中可能发生反应的化学方程式:
①_____;
②Li2O+H2SO4=Li2SO4+H2O。
(3)“洗涤”滤渣C时应该使用热水,其原因是_____。
(4)为了探究热酸浸提的最佳条件,将矿石在一定条件下酸浸4小时,测量锂元素浸出率的部分数据如表:
编号 | 矿酸比 | 硫酸浓度(%) | MgSO4用量(g) | 温度(℃) | 锂元素浸出率(%) |
1 | 1:1 | 90 | 0.00 | 100 | 70.34 |
2 | 1:1 | 98 | 0.00 | 100 | 73.89 |
3 | 1:1 | 98 | 0.00 | 150 | 78.24 |
4 | 1:3 | 98 | 0.00 | 200 | 85.53 |
5 | 1:3 | 98 | 1.25 | 250 | 90.26 |
6 | 1:3 | 98 | 2.50 | 250 | 95.88 |
①对比分析编号1和编号2的实验数据,可以得到的结论是_____。
②有同学想在实验6的基础上,从降低成本角度继续研究提高锂元素的浸出率,下面设计合理的是_____。
A 矿酸比1:2,硫酸浓度98%,MgSO4用量0.00,温度150℃
B 矿酸比1:2,硫酸浓度98%,MgSO4用量2.50,温度200℃
C 矿酸比1:2,硫酸浓度98%,MgSO4用量2.50,温度250℃
D 矿酸比1:3,硫酸浓度98%,MgSO4用量2.00,温度250℃