题目内容
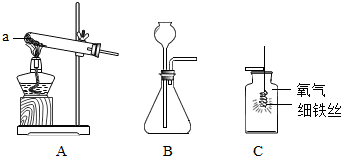
(2011?曲阜市模拟)(1)如图是化学实验中常用的几种装置.请回答下列问题:
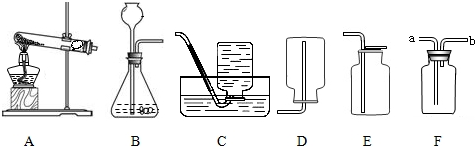
①利用上述B、E装置的组合可以制取的一种气体是
②小冬选用图中的装置制取CO2,他看到发生装置中有气泡冒出,然后把导气管插入到澄清的石灰水中,未观察到浑浊现象.其原因可能是(写出一条即可)
③F装置作为洗气瓶用于干燥某些气体,若干燥氧气,洗气瓶应装入的试剂是
(2)五一节后,小丽带着快乐的心情返回学校.当她来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了她的探究欲望.
[提出问题]这瓶NaOH溶液一定变质了,其变质程度如何呢?
[提出猜想]小丽的猜想:NaOH溶液部分变质.你的新猜想
[实验探究]小丽设计如下实验来验证自己的猜想,请根据表中内容填写小丽实验时的现象
假设你的猜想正确,并按小丽的实验方案进行实验,则你观察到的实验现象
[实验反思]
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是
(2)小丽第二次滴加的试剂除用指示剂外,还可以用
[拓展应用]保存NaOH溶液的方法是

①利用上述B、E装置的组合可以制取的一种气体是
氧气
氧气
,写出实验室制取该气体的化学反应方程式2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
| ||
②小冬选用图中的装置制取CO2,他看到发生装置中有气泡冒出,然后把导气管插入到澄清的石灰水中,未观察到浑浊现象.其原因可能是(写出一条即可)
盐酸的浓度过大,制得的CO2气体中含有HCl气体
盐酸的浓度过大,制得的CO2气体中含有HCl气体
③F装置作为洗气瓶用于干燥某些气体,若干燥氧气,洗气瓶应装入的试剂是
浓硫酸
浓硫酸
,进气口为a
a
(“a”或“b”).(2)五一节后,小丽带着快乐的心情返回学校.当她来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了她的探究欲望.
[提出问题]这瓶NaOH溶液一定变质了,其变质程度如何呢?
[提出猜想]小丽的猜想:NaOH溶液部分变质.你的新猜想
NaOH溶液全部变质
NaOH溶液全部变质
.[实验探究]小丽设计如下实验来验证自己的猜想,请根据表中内容填写小丽实验时的现象
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液. | 产生白色沉淀,酚酞试液变红 产生白色沉淀,酚酞试液变红 |
NaOH溶液部分变质 |
产生白色沉淀,酚酞试液不变色
产生白色沉淀,酚酞试液不变色
.[实验反思]
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是
③④
③④
(填序号).(2)小丽第二次滴加的试剂除用指示剂外,还可以用
硫酸铜溶液
硫酸铜溶液
替代.[拓展应用]保存NaOH溶液的方法是
密封保存
密封保存
.分析:根据已有的知识进行分析,气体发生装置的选择取决于反应物的状态和反应的条件,收集装置的选择取决于气体的密度和水溶性,根据浓硫酸的吸水性,可以用作干燥剂,氢氧化钠容易与空气中的二氧化碳反应而变质,生成碳酸钠,要检验变质的程度,需要检验是否含有氢氧化钠,也就是需要除去碳酸钠再检验,据此解答即可.
解答:解:(1)B①装置是固液常温下的反应,E是向上排空气法收集气体,组合可以制取氧气,使用的药品时过氧化氢溶液和二氧化锰,故填:氧气,2H2O2
2H2O+O2↑;
②制取的二氧化碳不能使澄清的石灰水变浑浊,可是使用的盐酸浓度过大,导致二氧化碳气体中含有氯化氢气体,故填:盐酸的浓度过大,制得的CO2气体中含有HCl气体;
③浓硫酸具有吸水性,可以用作干燥剂,氧气需要充分通过浓硫酸,进气口为a,故填:浓硫酸,a;
(2)【提出猜想】氢氧化钠可能是全部变质,故填:NaOH溶液全部变质;
【实验探究】氯化钙能与碳酸钠反应生成氯化钠和碳酸钙白色沉淀,若含有氢氧化钠,则酚酞试液会变红,若无氢氧化钠,则酚酞试液不变色,故填:产生白色沉淀,酚酞试液变红;产生白色沉淀,酚酞试液不变色;
【实验反思】
(1)要证明是部分变质,则反应后不能生成显碱性的物质,氢氧化钙和氢氧化钡与碳酸钠反应会生成氢氧化钠,影响对氢氧化钠的检验,故填:③④;
(2)要证明含有氢氧化钠,还可以使用硫酸铜溶液,硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀,故填:硫酸铜溶液.
【拓展应用】根据实验可以看出,氢氧化钠应该密封保存,防止变质,故填:密封保存.
| ||
②制取的二氧化碳不能使澄清的石灰水变浑浊,可是使用的盐酸浓度过大,导致二氧化碳气体中含有氯化氢气体,故填:盐酸的浓度过大,制得的CO2气体中含有HCl气体;
③浓硫酸具有吸水性,可以用作干燥剂,氧气需要充分通过浓硫酸,进气口为a,故填:浓硫酸,a;
(2)【提出猜想】氢氧化钠可能是全部变质,故填:NaOH溶液全部变质;
【实验探究】氯化钙能与碳酸钠反应生成氯化钠和碳酸钙白色沉淀,若含有氢氧化钠,则酚酞试液会变红,若无氢氧化钠,则酚酞试液不变色,故填:产生白色沉淀,酚酞试液变红;产生白色沉淀,酚酞试液不变色;
【实验反思】
(1)要证明是部分变质,则反应后不能生成显碱性的物质,氢氧化钙和氢氧化钡与碳酸钠反应会生成氢氧化钠,影响对氢氧化钠的检验,故填:③④;
(2)要证明含有氢氧化钠,还可以使用硫酸铜溶液,硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀,故填:硫酸铜溶液.
【拓展应用】根据实验可以看出,氢氧化钠应该密封保存,防止变质,故填:密封保存.
点评:本题考查了实验室气体的制取以及变质物质成分的探究,完成此题,可以依据已有的知识进行.要求同学们熟练掌握气体发生装置的选择以及收集装置的选择依据,以便灵活应用.

练习册系列答案
相关题目
 (2011?曲阜市模拟)如图A、B、C为三种物质的溶解度曲线,据图回答:
(2011?曲阜市模拟)如图A、B、C为三种物质的溶解度曲线,据图回答: (2011?曲阜市模拟)去年冬天至今年春天,我省遭遇大范围持续干旱.
(2011?曲阜市模拟)去年冬天至今年春天,我省遭遇大范围持续干旱.