题目内容
(2013河南)酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应。
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有 生成。
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象。取反应后的部分溶液加热、蒸干、得到白色固体。
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性。请填写下表:
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点。
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质。
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶。请回答:
①溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在蒸发操作中的作用是什么?
②加入Na2CO3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充。
(4)LiOH和NaOH的化学性质相似。“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量。请计算:用LiOH完全吸收176 g CO2生成Li2CO3和H2O,理论上至少需要LiOH的质量是多少?
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有 生成。
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象。取反应后的部分溶液加热、蒸干、得到白色固体。
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性。请填写下表:
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 | pH>7 | |
| | CaCl2 |
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质。
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶。请回答:
| 部分物质的溶解性表(室温) | ||||
| | OH- | Cl- | SO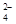 | CO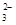 |
| H+ | | 溶、挥 | 溶 | 溶、挥 |
| Ba2+ | 溶 | 溶 | 不溶 | 不溶 |
| Ca2+ | 微溶 | 溶 | 微溶 | 不溶 |
| Mg2+ | 不溶 | 溶 | 溶 | 微溶 |
②加入Na2CO3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充。
(4)LiOH和NaOH的化学性质相似。“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量。请计算:用LiOH完全吸收176 g CO2生成Li2CO3和H2O,理论上至少需要LiOH的质量是多少?
(1)水(或难电离物)

①用玻璃棒不断搅拌,防止因局部温度过高造成液滴飞溅 ②除去CaCl2杂质和过量的BaCl2
③过量的NaOH和Na2CO3未除去,还应加入适量的盐酸 (4) 192g

①用玻璃棒不断搅拌,防止因局部温度过高造成液滴飞溅 ②除去CaCl2杂质和过量的BaCl2
③过量的NaOH和Na2CO3未除去,还应加入适量的盐酸 (4) 192g
试题分析:复分解反应的条件是两种化合物相互交换成份后要有水、气体或沉淀生成;用PH试纸测量溶液的PH值,不能直接将PH试纸伸入待测溶液中,而是用玻璃棒蘸取少量待测溶液凃在PH试纸上;根据溶液显示的PH值确定其酸碱性,以确定溶质的成份;溶解、过滤和蒸发的过程中都要用到玻璃棒,在蒸发的过程中玻璃棒的作用主要是搅拌,使其均匀受热,避免因局部溫度过高而造成液滴飞溅;碳酸钠可与氯化钙和氯化钡反应,主要用于除去溶液中的氯化钙和氢化钡等物质,该实验设计不够严密,过量的氢氧化钠和剩余的碳酸钠无法除去,结晶之后样品中仍然含有杂质.
(4)解:设理论上至少需要。011的质重为3£
2LiOH + CO2 = Li2CO3 + H2O
48 44
X 176g
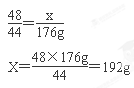
答:理论上需要匕10?1的质重为1928

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目