题目内容
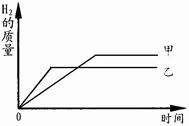
把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的锌和铁,反应后金属都没有剩余。产生H2的质量随时间变化的趋势如图。下列说法正确的是( )

| A.甲代表锌、乙代表铁 |
| B.甲的反应速度比乙快 |
| C.反应消耗等质量的硫酸 |
| D.与铁反应的稀硫酸可能恰好用完 |
D
A.从图示可以看出,从斜线可以看出同一时间内乙产生的氢气多,说明乙的金属活动性要比甲强,金属活动性Zn>Fe,故A说法错误;
B.从图示可知,从斜线可以看出同一时间内乙产生的氢气要比甲多,即乙的反应速度要比甲快,故B说法错误;
C. 由图示可知,最后生成氢气的质量不同说明消耗酸的质量不同,因为氢气来源于酸中的氢,故C说法错误;
D.等质量的锌和铁两种金属,与等体积等浓度的酸反应后金属都没有剩余,说明酸是足量的,通过化学方程式可知等质量的锌和铁与足量的酸反应金属铁消耗的酸多,故D说法正确。
B.从图示可知,从斜线可以看出同一时间内乙产生的氢气要比甲多,即乙的反应速度要比甲快,故B说法错误;
C. 由图示可知,最后生成氢气的质量不同说明消耗酸的质量不同,因为氢气来源于酸中的氢,故C说法错误;
D.等质量的锌和铁两种金属,与等体积等浓度的酸反应后金属都没有剩余,说明酸是足量的,通过化学方程式可知等质量的锌和铁与足量的酸反应金属铁消耗的酸多,故D说法正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目