题目内容
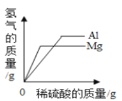
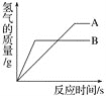
【题目】等质量的AB两种金属,分别与质量分数相同的足量的稀盐酸反应(已知,AB在生成物中均为+2价),生成氢气的质量随反应时间的变化关系如图所示,下列判断正确的是()
A. 金属活动性顺序:A>B
B. 相对原子质量:A>B
C. 反应结束后,所得溶液质量:A>B
D. 反应结束后,生成氢气质量:A>B
【答案】D
【解析】
A、观察图像可知,与酸反应,B比A快,故金属活动性顺序是B>A,选项A错误;
B、生成物中,两种金属均显示+2价,根据化学反应中金属与氢气的质量比关系可知,相对原子质量越大,产生的氢气越少,由图可知,产生氢气的质量关系:A>B,因此相对原子质量:A<B ,选项B错误;
C、根据质量守恒定律可知,反应后所得溶液的质量=稀盐酸的质量+参加反应的金属的质量-氢气的质量,由题干可知,稀盐酸的质量相等,加入的金属质量相等,产生氢气的质量A>B,故所得溶液质量关系为A<B,选项C错误;
D、从图可以看出,反应结束后,生成氢气质量:A>B。选项D正确。故选D。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目