题目内容
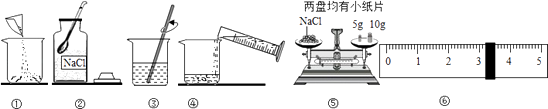
【题目】请根据下列实验图1回答问题: 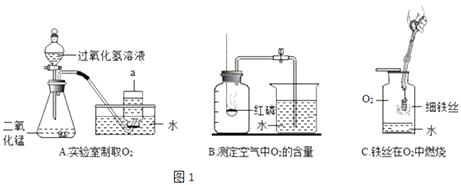
(1)仪器a的名称是 .
(2)上述三个实验中,水对实验仪器起到安全保护作用的是(填字母)
(3)写出A实验中发生反应的化学方程式;
(4)对于B实验,①该实验中,红磷需稍过量,目的是②待燃烧停止,白烟消失并冷却至室温后,打开止水夹,观察到烧杯中水进入集气瓶,瓶内水面最终上升约至1刻度处,由此可知氧气约占空气总体积的由本实验还可推知氮气的某些性质,请你写出其中的一种:
(5)小李同学进行了改进与创新,实验过程如图2所示: 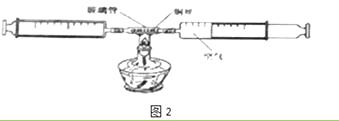
① 该装置也可用于测量空气中氧气的含量,其实验原理用化学方程式可表示为;
②使用该装置进行实验时需交替缓慢推动两个注射器活塞的原因是 , 实验结束后移开酒精灯,恢复到室温后读数即可计算出氧气含量,该装置的优点是(任写一点).
【答案】
(1)集气瓶
(2)C
(3)2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
(4)将容器内氧气全部消耗尽;![]() ;氮气不支持燃烧
;氮气不支持燃烧
(5)2Cu+O2 ![]() 2CuO;注射器内氧气与铜粉充分反应;反应始终在密闭器中进行,测量结果更准确
2CuO;注射器内氧气与铜粉充分反应;反应始终在密闭器中进行,测量结果更准确
【解析】解:(1)图中所示仪器是集气瓶,故填:集气瓶;(2)A实验中,水的作用是用排水法收集气体,B实验中,水的作用是用水的体积来验证氧气的体积,C实验中,水的作用是防止高温溅落物炸裂瓶底,故选C;(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2 ![]() 2H2O+O2↑;(4)①该实验中红磷稍过量,目的是将空气中氧气完全反应;
2H2O+O2↑;(4)①该实验中红磷稍过量,目的是将空气中氧气完全反应;
②待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶容积的五分之一,说明氧气约占空气总体积的五分之一;水倒流入集气瓶中的体积只有五分之一,若氮气易溶于水,则倒流入瓶内的水几乎会充满整个集气瓶,因此氮气是难溶于水的;红磷燃烧一会熄灭了,说明氮气不燃烧不支持燃烧,其化学性质不活泼等;(5)①铜被加热生成氧化铜,其实验原理用化学方程式可表示为:2Cu+O2 ![]() 2CuO;
2CuO;
②在实验的加热过程中,交替缓慢推动两个注射器活塞的目的是使注射器内氧气与铜粉充分反应.实验结束后移开酒精灯,恢复到室温后读数即可计算出氧气含量,B装置的优点是反应始终在密闭容器中进行,测量结果更准确;
如图2改进实验与B实验相比,明显的优点是,装置简单或操作简便或实验结果更准确(误差小),或封闭体系更环保或试验成功率高等,故填:装置简单或操作简便或实验结果更准确(误差小),或封闭体系更环保或试验成功率高等;
所以答案是:(1)集气瓶;(2)C;(3)2H2O2 ![]() 2H2O+O2↑;(4)①将容器内氧气全部消耗尽; ②
2H2O+O2↑;(4)①将容器内氧气全部消耗尽; ② ![]() ;氮气不支持燃烧;(5)①2Cu+O2
;氮气不支持燃烧;(5)①2Cu+O2 ![]() 2CuO;②注射器内氧气与铜粉充分反应; 反应始终在密闭器中进行,测量结果更准确.
2CuO;②注射器内氧气与铜粉充分反应; 反应始终在密闭器中进行,测量结果更准确.
【考点精析】掌握氧气的化学性质和氧气的制取装置是解答本题的根本,需要知道氧气的化学性质:特有的性质:支持燃烧,供给呼吸;发生装置:固固加热型、固液不加热型.

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案