题目内容
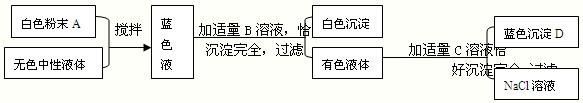
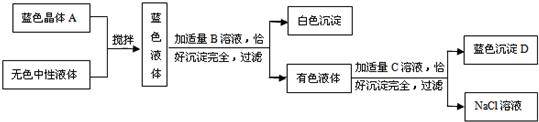
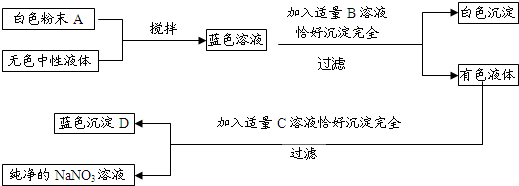
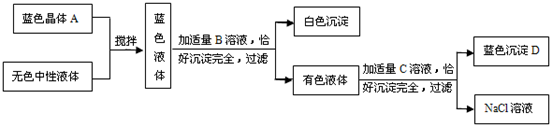
已知常用的强酸(H2SO4、HCl、HNO3)跟常用的强碱(NaOH、KOH)反应生成的盐的水溶液显中性,现将某白色粉末溶入一无色中性液体中,按以下图示进行实验.
试按下列要求推断未知物:(1)用化学式写出:B ;C ;D .
(2)若A是纯净物,无色中性液体也是纯净物,则中性液体是 .(填化学式)
(3)若A是纯净物,无色中性液体是只含一种溶质的溶液,则中性液体是 溶液或 溶液.(填化学式)
【答案】分析:根据沉淀D的颜色为蓝色,可判断沉淀D为氢氧化铜;
根据蓝色溶液的颜色可判断蓝色溶液为可溶性铜盐,而该蓝色溶液与B溶液恰好完全反应后生成白色沉淀和有色溶液的特点,可知有色溶液仍为蓝色溶液中仍含有铜离子,又该溶液与C溶液恰好完全反应时生成氢氧化铜沉淀和纯净的硝酸钠溶液,根据复分解反应交换成分的特点,可推断形成氢氧化铜沉淀的氢氧根来自C溶液,生成物硝酸钠中的硝酸根应来自于有色溶液.综上所述可得:有色溶液为硝酸铜溶液;
硝酸铜与碱类物质C的溶液恰好完全反应生成氢氧化铜沉淀和纯净的硝酸钠溶液,则物质C为氢氧化钠;
硝酸铜溶液是由蓝色溶液与B溶液反应所形成的,根据复分解反应交换成分的特点,则硝酸铜中的硝酸根来自溶液B;则蓝色溶液一定不是硝酸铜溶液,可溶性铜盐还有氯化铜和硫酸铜,氯化铜溶液呈蓝绿色,则蓝色溶液为硫酸铜溶液;蓝色硫酸铜溶液由白色粉末和无色中性液体而形成,无色中性液体中不含铜,则蓝色溶液中的铜元素应来自白色粉末,含铜元素的白色粉末为硫酸铜(氯化铜粉末的颜色在初中化学中没及提及,故在此不做考虑而排除),所以蓝色溶液为硫酸铜溶液;硫酸铜溶液与硝酸钡溶液反应才能生成白色沉淀和硝酸铜,则B为硝酸钡.
解答:解:(1)物质B为硝酸钡,其化学式为Ba(NO3)2;C物质为氢氧化钠,化学式为NaOH;D物质为氢氧化铜,化学式为Cu(OH)2;
故选Ba(NO3)2,NaOH,Cu(OH)2;
(2)无色中性液体为纯净物,该液体与纯净物A形成硫酸铜溶液,则无色中性液体为水,溶解硫酸铜粉末得到蓝色溶液硫酸铜溶液;
故答:H2O;
(3)无色中性液体是只含一种溶质的溶液,根据最终得到纯净的硝酸钠溶液的需要,又纯净物A为硫酸铜,形成溶液后硫酸根可以被硝酸钡全部沉淀,并且最终形成纯净硝酸钠溶液,所以无色中性溶液中可以含有硫酸钠或硝酸钠,所以只含一种溶质的溶液为硝酸钠的中性溶液或硫酸钠的中性溶液;
故答:NaNO3,Na2SO4.
点评:氯化铜溶液中含有Cl-和Cu2+,溶液中含Cu2+时溶液呈蓝色,而CuCl2溶液受Cl-的影响,溶液呈蓝绿色而非蓝色.
根据蓝色溶液的颜色可判断蓝色溶液为可溶性铜盐,而该蓝色溶液与B溶液恰好完全反应后生成白色沉淀和有色溶液的特点,可知有色溶液仍为蓝色溶液中仍含有铜离子,又该溶液与C溶液恰好完全反应时生成氢氧化铜沉淀和纯净的硝酸钠溶液,根据复分解反应交换成分的特点,可推断形成氢氧化铜沉淀的氢氧根来自C溶液,生成物硝酸钠中的硝酸根应来自于有色溶液.综上所述可得:有色溶液为硝酸铜溶液;
硝酸铜与碱类物质C的溶液恰好完全反应生成氢氧化铜沉淀和纯净的硝酸钠溶液,则物质C为氢氧化钠;
硝酸铜溶液是由蓝色溶液与B溶液反应所形成的,根据复分解反应交换成分的特点,则硝酸铜中的硝酸根来自溶液B;则蓝色溶液一定不是硝酸铜溶液,可溶性铜盐还有氯化铜和硫酸铜,氯化铜溶液呈蓝绿色,则蓝色溶液为硫酸铜溶液;蓝色硫酸铜溶液由白色粉末和无色中性液体而形成,无色中性液体中不含铜,则蓝色溶液中的铜元素应来自白色粉末,含铜元素的白色粉末为硫酸铜(氯化铜粉末的颜色在初中化学中没及提及,故在此不做考虑而排除),所以蓝色溶液为硫酸铜溶液;硫酸铜溶液与硝酸钡溶液反应才能生成白色沉淀和硝酸铜,则B为硝酸钡.
解答:解:(1)物质B为硝酸钡,其化学式为Ba(NO3)2;C物质为氢氧化钠,化学式为NaOH;D物质为氢氧化铜,化学式为Cu(OH)2;
故选Ba(NO3)2,NaOH,Cu(OH)2;
(2)无色中性液体为纯净物,该液体与纯净物A形成硫酸铜溶液,则无色中性液体为水,溶解硫酸铜粉末得到蓝色溶液硫酸铜溶液;
故答:H2O;
(3)无色中性液体是只含一种溶质的溶液,根据最终得到纯净的硝酸钠溶液的需要,又纯净物A为硫酸铜,形成溶液后硫酸根可以被硝酸钡全部沉淀,并且最终形成纯净硝酸钠溶液,所以无色中性溶液中可以含有硫酸钠或硝酸钠,所以只含一种溶质的溶液为硝酸钠的中性溶液或硫酸钠的中性溶液;
故答:NaNO3,Na2SO4.
点评:氯化铜溶液中含有Cl-和Cu2+,溶液中含Cu2+时溶液呈蓝色,而CuCl2溶液受Cl-的影响,溶液呈蓝绿色而非蓝色.

练习册系列答案
相关题目