题目内容
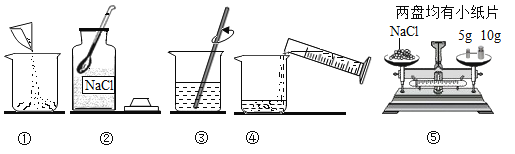
【题目】如果配制6%的氯化钠溶液的溶质质量分数偏小,其原因是
A. 称取的氯化钠固体质量偏大
B. 转移称量好的氯化钠固体时,有少量洒落在桌面上
C. 量取水的体积偏小
D. 转移配制好的溶液时,有少量液体溅出
【答案】B
【解析】如果配制6%的氯化钠溶液的溶质质量分数偏小,其原因是氯化钠的质量偏少或水的量偏多。称取的氯化钠固体质量偏大,会使溶质质量分数偏大;转移称量好的氯化钠固体时,有少量洒落在桌面上,氯化钠溶液的溶质质量分数偏小;量取水的体积偏小,氯化钠溶液的溶质质量分数偏大D. 转移配制好的溶液时,有少量液体溅出,不影响氯化钠溶液的溶质质量分数。故选B

练习册系列答案
相关题目
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
①为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%H2O2溶液与1.0g MnO2均匀混合
Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学(符号)表达式是 _;Ⅱ中x的值应为 。
②乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
Ⅲ | 50.0g | 4% | 0.1g | 31 mL |
本实验中,测量O2体积的装置是____________(填编号)。

实验结论:在相同条件下, ,双氧水分解得越快。
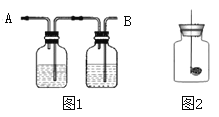
丙用下图装置进行实验,通过比较 也能达到实验目的。