题目内容
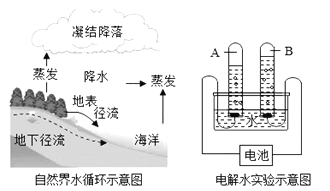
【题目】氟化钠是某些牙膏的添加剂,能有效预防龋齿.(1)图Ⅰ是氟元素在元素周期表中的相关信息,则氟元素的相对原子质量是________。
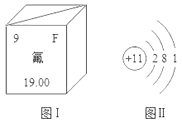
图Ⅱ是钠原子结构示意图,由此可知钠原子的核外电子数为_______,在化学反应中易________(填“失”或“得”)电子,形成_______(写粒子符号)。
(2)氟化钠可以用钠与氟气(F2)化合反应制得,氟气和氢气一样,都是由_______(填“分子”、“原子”或“离子”)构成。
【答案】19.00 11 失 Na+ 分子
【解析】
(1)根据氟元素在元素周期表中的相关信息,氟元素的原子序数是9,相对原子质量为19.00;根据钠原子结构示意图,可知钠原子的最外层的电子数为1,没有达到稳定结构,易失去1个电子达到8电子的稳定结构,形成Na+。
(2)氢气是由氢分子构成的,氟气和氢气一样,是由分子构成的。

 名校课堂系列答案
名校课堂系列答案【题目】多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界
(1)根据下表提供的信息,填写有关含碳物质的对应特性.
物质用途 | 石墨作电极 | 金刚石切割玻璃 |
对应性质 | _______ | ________ |
(2)液态二氧化碳灭火器可用于扑救档案资料室发生的火灾,
下列说法正确的有__ (填字母).
A.液态二氧化碳气化时吸热,降低了周围的温度
B.二氧化碳不能燃烧,也不能支持燃烧
C.液态二氧化碳气化后不会污染档案资料
(3)二氧化碳是导致地球上发生“温室效应”的主要气体,现代入类已意识到它的排放必须控制.空气中二氧化碳的主要来源是__,为了减缓大气中二氧化碳含量的增加,以下建议合理的是__ (填序号).
①开发太阳能、水能、风能、地热等能源;②减少化石燃料的使用;③大量植树种草,禁止乱砍滥伐.
(4)天然气的主要成分是甲烷,它是一种“清洁能源”.甲烷在空气中燃烧生成二氧化碳和水,写出甲烷燃烧的化学方程式__.
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等; 猜想2:相等。
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
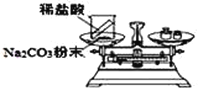
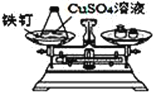
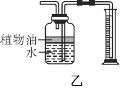
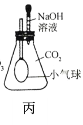
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面 ______,溶液____,天平指针___偏转。 |
结论 | 猜想1正确。有关反应的方程式是:Na2CO3+2HCl | 猜想2正确。反应的化学方程式:__________________ |
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在___容器中进行。
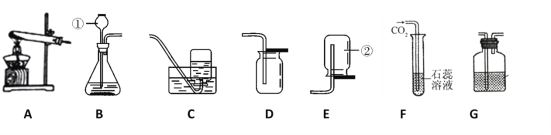
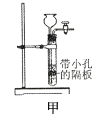
(优化装置)同学们对甲组左盘中的反应装置进行了如下两种改进,
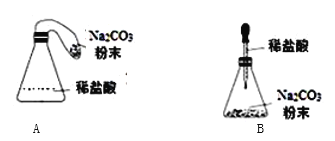
你认为最佳装置是______(填序号),理由是__________。
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想二正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论是:___的各物质的质量总和等于反应后生成的各物质的质量总和。
(解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由______种元素组成。