题目内容
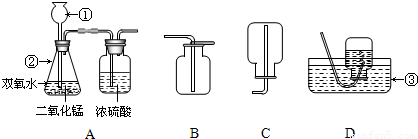
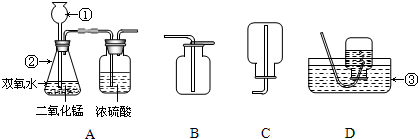
下面所示为实验室中二氧化碳制备、干燥和收集的部分仪器.试根据题目要求,回答下列问题:
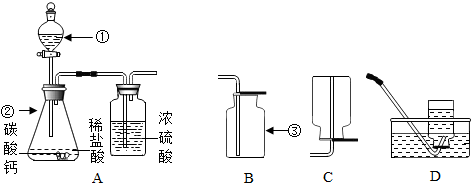
(1)写出图中所标示的实验仪器名称:
①
(2)用碳酸钙和稀盐酸为原料在实验室中制备并收集干燥的二氧化碳.
①所选仪器的连接顺序为
②写出碳酸钙和稀盐酸为原料制取二氧化碳的化学方程式:
③A装置中盛有浓硫酸的洗气瓶的作用是
(3)氢气气体难溶于水,密度小于空气,实验室收集氢气的方法有

(1)写出图中所标示的实验仪器名称:
①
分液漏斗
分液漏斗
;②锥形瓶
锥形瓶
;③集气瓶
集气瓶
.(2)用碳酸钙和稀盐酸为原料在实验室中制备并收集干燥的二氧化碳.
①所选仪器的连接顺序为
A→B
A→B
(填写仪器字母).证明二氧化碳已经收集满的方法是将燃着的木条
燃着的木条
放在集气瓶口
集气瓶口
,如果看到木条熄灭
木条熄灭
则证明集气瓶内已经充满二氧化碳.②写出碳酸钙和稀盐酸为原料制取二氧化碳的化学方程式:
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.③A装置中盛有浓硫酸的洗气瓶的作用是
干燥
干燥
.(3)氢气气体难溶于水,密度小于空气,实验室收集氢气的方法有
C
C
和D
D
(填写仪器序号).分析:(1)根据常见的化学仪器的名称进行分析解答.
(2)①收集干燥的二氧化碳气体,所以要先制取,再干燥,再收集;根据二氧化碳的验满方法进行分析解答.
②碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,写出反应的化学方程式即可.
③根据浓硫酸具有吸水性,进行分析解答.
(3)氢气气体难溶于水,密度小于空气,据此可以确定收集方法.
(2)①收集干燥的二氧化碳气体,所以要先制取,再干燥,再收集;根据二氧化碳的验满方法进行分析解答.
②碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,写出反应的化学方程式即可.
③根据浓硫酸具有吸水性,进行分析解答.
(3)氢气气体难溶于水,密度小于空气,据此可以确定收集方法.
解答:解:(1)仪器①是分液漏斗;仪器②是锥形瓶,仪器③是集气瓶.
(2)①A装置是用来制取二氧化碳的装置,由于浓硫酸具有吸水性,可以用来干燥气体,再进行收集,由于要收集干燥的二氧化碳,根据密度比空气大,用向上排空气法收集,所以仪器的连接顺序为A→B.
检验二氧化碳已经收集满的方法是将燃着的木条放在集气瓶口,如果看到木条熄灭,则证明集气瓶内已经充满二氧化碳.
②碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
③浓硫酸具有吸水性,A装置中盛有浓硫酸的洗气瓶的作用干燥二氧化碳气体.
(3)氢气的密度比空气小,可以采用向下排空气法收集;氢气难溶于水,也可以采用排水法收集.
故答案为:(1)①分液漏斗,②锥形瓶,③集气瓶;(2)①A→B;燃着的木条;集气瓶口;木条熄灭;②CaCO3+2HCl=H2O+CaCl2+CO2↑;③干燥;(3)C;D.
(2)①A装置是用来制取二氧化碳的装置,由于浓硫酸具有吸水性,可以用来干燥气体,再进行收集,由于要收集干燥的二氧化碳,根据密度比空气大,用向上排空气法收集,所以仪器的连接顺序为A→B.
检验二氧化碳已经收集满的方法是将燃着的木条放在集气瓶口,如果看到木条熄灭,则证明集气瓶内已经充满二氧化碳.
②碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
③浓硫酸具有吸水性,A装置中盛有浓硫酸的洗气瓶的作用干燥二氧化碳气体.
(3)氢气的密度比空气小,可以采用向下排空气法收集;氢气难溶于水,也可以采用排水法收集.
故答案为:(1)①分液漏斗,②锥形瓶,③集气瓶;(2)①A→B;燃着的木条;集气瓶口;木条熄灭;②CaCO3+2HCl=H2O+CaCl2+CO2↑;③干燥;(3)C;D.
点评:本题难度不是很大,是中考的重要考点之一,熟练掌握实验室中制取二氧化碳气体的反应原理、发生装置和收集装置的选择依据是正确解答本题的关键.

练习册系列答案
相关题目
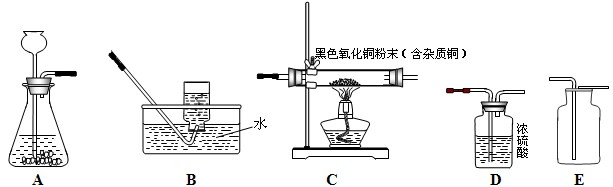
 Cu+H2O;D1、D2、D3为3个浓硫酸洗气瓶)
Cu+H2O;D1、D2、D3为3个浓硫酸洗气瓶)