题目内容
【题目】用化学用语填空:
(1)人体中含量最高的金属元素:;
(2)三个氮原子:;
(3)二个铁离子:;
(4)二氧化硫中硫元素的化合价:;
(5)干冰的化学式:;
(6)赤铁矿主要成分的化学式: .
【答案】
(1)Ca
(2)3N
(3)2Fe3+
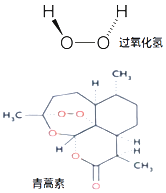
(4)![]() O2
O2
(5)CO2
(6)Fe2O3
【解析】解:(1)人体中含量最高的金属元素是钙元素,其元素符号为Ca.(2)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故三个氮原子表示为:3N.(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.二个铁离子可表示为2Fe3+ . (4)二氧化硫中氧元素显﹣2价,硫元素的化合价为+4价;由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故二氧化硫中硫元素的化合价可表示为: ![]() O2 . (5)干冰是固态的二氧化碳,其化学式为:CO2 . (6)赤铁矿主要成分是氧化铁,其化学式为:Fe2O3 . 所以答案是:(1)Ca;(2)3N;(3)2Fe3+;(4)
O2 . (5)干冰是固态的二氧化碳,其化学式为:CO2 . (6)赤铁矿主要成分是氧化铁,其化学式为:Fe2O3 . 所以答案是:(1)Ca;(2)3N;(3)2Fe3+;(4) ![]() O2;(5)CO2;(6)Fe2O3 .
O2;(5)CO2;(6)Fe2O3 .

 科学实验活动册系列答案
科学实验活动册系列答案【题目】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.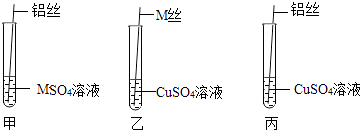
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
(1)【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是 .
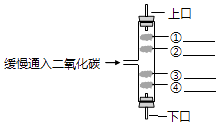
(2)【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸),根据实验现象,完成表中的实验结论:
实验操作 | M丝插入试管①中 | 钢丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
刚开始的现象 | 有少量气泡产生 | 无气 | 无气泡 | M>Cu: |
几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
(3)【交流与表达】同学们对上述实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因是 .
(4)【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
①试管乙中观察到的现象是 .
②试管丙中反应的化学方程式为 .
(5)【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管(填试管编号)中的实验,也可以得出正确的结论.