题目内容
A、B、C、D、E分别是镁片(无锈)、氯化铜溶液、氢氧化钠溶液、氧化铜粉末、稀盐酸中的一种物质,用两个圆圈相切表示两种物质在常温下能反应,且A与B反应无现象,A与C反应生成D溶液.请回答下列问题:

(1)在A、B周围画出C、D、E,并将物质名称(或化学式)标在圆中
(2)写出B和D反应的化学方程式 ;
(3)描述A与E反应的实验现象为 。
【答案】
故答案为:(1)
(2)CuCl2+2NaOH=Cu(OH)2↓+2NaCl
(3)银白色金属表面(迅速)产生气泡,并逐渐变小(消失),放出热量.
【解析】
试题分析:
(1)五种物质中盐酸与氢氧化钠反应无明显现象,盐酸与氧化铜反应生成氯化铜,因此A为盐酸,B为氢氧化钠,C为氧化铜,D为氯化铜,E为镁.如图所示:
(2)B是氢氧化钠,D为氯化铜,氢氧化钠和氯化铜反应生成氢氧化铜沉淀和氯化钠,化学方程式为CuCl2+2NaOH=Cu(OH)2↓+2NaCl
(3)由于镁能与盐酸反应生成氢气,所以A与E反应的实验现象为银白色金属表面(迅速)产生气泡,并逐渐变小(消失),放出热量.
考点:物质的鉴别、推断.

练习册系列答案
相关题目
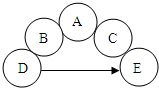 A、B、C、D、E分别是一氧化碳、二氧化碳、三氧化二铁、稀硫酸和氢氧化钠溶液中的一种物质.用五个圆表示五种物质,用两圆相切表示两种物质可以发生化学反应,“一”表示两物质间的转化关系(部分反应物、生成物和反应条件已略去),且物质D转化成物质E的过程中吸热.请回答下列问题:
A、B、C、D、E分别是一氧化碳、二氧化碳、三氧化二铁、稀硫酸和氢氧化钠溶液中的一种物质.用五个圆表示五种物质,用两圆相切表示两种物质可以发生化学反应,“一”表示两物质间的转化关系(部分反应物、生成物和反应条件已略去),且物质D转化成物质E的过程中吸热.请回答下列问题: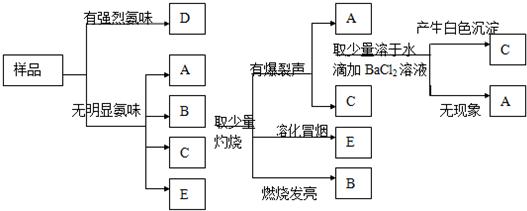
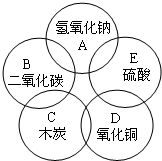 A、B、C、D、E分别是二氧化碳、木炭、氧化铜、稀硫酸、氢氧化钠溶液中的一种物质,用两圆相交表示两种物质可以发生反应,回答下列问题.
A、B、C、D、E分别是二氧化碳、木炭、氧化铜、稀硫酸、氢氧化钠溶液中的一种物质,用两圆相交表示两种物质可以发生反应,回答下列问题.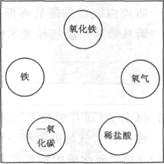 (2009?哈尔滨)A、B、C、D、E分别是氧化铁、铁、氧气、一氧化碳、稀盐酸中的一种物质.请回答下列问题:
(2009?哈尔滨)A、B、C、D、E分别是氧化铁、铁、氧气、一氧化碳、稀盐酸中的一种物质.请回答下列问题: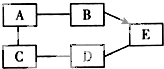 A、B、C、D、E分别是初中化学不同类别的常见物质,其中C的水溶液呈蓝色,E的增加使全球气候变暖.它们之间关系如图所示(“-”表示相连的物质能发生反应,“→”表示一种物质可转化为另一种物质).请回答下列问题“
A、B、C、D、E分别是初中化学不同类别的常见物质,其中C的水溶液呈蓝色,E的增加使全球气候变暖.它们之间关系如图所示(“-”表示相连的物质能发生反应,“→”表示一种物质可转化为另一种物质).请回答下列问题“