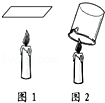
题目内容
在过氧化氢溶液的分解反应中,二氧化锰能作催化剂。下列有关催化剂的说法正确的是 (选填序号)。
A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量 D.能改变化学反应速率
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。
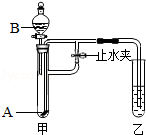
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①的目的是 。
(3)步骤④对应的实验操作是 ,需用到的玻璃仪器有 。
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铜对过氧化氢溶液分解的催化作用,其中观察效果最差的是 (选填序号)。
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量 D.能改变化学反应速率
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| ,带火星的木条复燃 | | | 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂 |
(2)步骤①的目的是 。
(3)步骤④对应的实验操作是 ,需用到的玻璃仪器有 。
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铜对过氧化氢溶液分解的催化作用,其中观察效果最差的是 (选填序号)。
 | 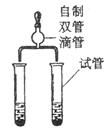 |  |  |
| 第一组 | 第二组 | 第三组 | 第四组 |
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
D
【进行实验】
(1)有大量气泡产生 固体质量仍为0.2g
将固体加入盛有5mL5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象
(2)与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化
(3)过滤 烧杯、玻璃棒、漏斗
【拓展探究】C
【进行实验】
(1)有大量气泡产生 固体质量仍为0.2g
将固体加入盛有5mL5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象
(2)与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化
(3)过滤 烧杯、玻璃棒、漏斗
【拓展探究】C
试题分析:
催化剂是指能改变其他物质的化学反应速率,而质量和化学性质保持不变的物质。对照该定义,答案选D。
【进行实验】
(1)根据实验结论“在过氧化氢溶液的分解反应中,氧化铜也能作催化剂”,结合催化剂的定义,我们可以知道步骤③实验现象为:有大量气泡产生。此步是验证了氧化铜“能改变其他物质的化学反应速率”这一点。步骤⑥结果固体质量仍为0.2g,此步是验证了氧化铜“质量不变”这一点。步骤⑦操作是为了验证氧化铜“化学性质不变”,所以采取的操作为:将固体加入盛有5mL5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象。
(2)与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化。
(3)步骤④后固体与液体发生了分离,固体被分离出来了,此操作为过滤。过滤用到的仪器有:烧杯、玻璃棒、漏斗。
【拓展探究】第三组中,由于氧化铜与二氧化锰都对过氧化氢的分解起催化作用,故带火星的木条都能复燃,两者现象对比并不明显,故答案选C。

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目