题目内容
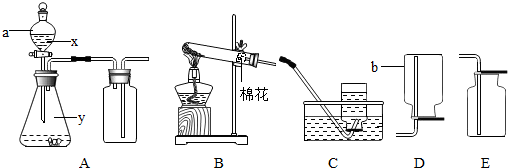
活动小组同学用加热草酸晶体制得的CO(H2C2O4?2H2O═CO↑+CO2↑+3H2O),做炼铁原理实验并进行尾气处理,设计以下装置(图甲、图乙).回答下列有关问题:
(1)为了获得干燥纯净的CO,A、B两装置中应分别存放 、浓硫酸
(2)硬质玻璃管中发生反应的化学方程式
(3)选择图甲处理尾气,实验时应先点燃 (填“a”或“b”)处的酒精灯.理由是 .图乙与图甲所示的尾气处理方法相比较,其主要优点是
(4)活动小组的同学通过查阅资料得知:常温下,CO能与氯化钯PdCl2溶液反应.于是他们选择了将尾气直接通入氯化钯溶液中进行处理.该反应的化学方程式为:CO+PdCl2+H2O═Pd↓+CO2+2R,其中R的化学式为 .此法与上述方法相比除了具有图乙比图甲所示方法的优点外,从实验角度看它还有的优点是
(写出一条合理答案即可)

(1)为了获得干燥纯净的CO,A、B两装置中应分别存放
(2)硬质玻璃管中发生反应的化学方程式
(3)选择图甲处理尾气,实验时应先点燃
(4)活动小组的同学通过查阅资料得知:常温下,CO能与氯化钯PdCl2溶液反应.于是他们选择了将尾气直接通入氯化钯溶液中进行处理.该反应的化学方程式为:CO+PdCl2+H2O═Pd↓+CO2+2R,其中R的化学式为
考点:一氧化碳还原氧化铁,常见气体的检验与除杂方法,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)氢氧化钠溶液能够吸收二氧化碳;
(2)高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳;
(3)一氧化碳有毒,扩散到空气中会污染环境;
(4)化学反应前后,元素的种类不变,原子的种类、总个数不变;
不同的实验方法,有不同的优缺点.
(2)高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳;
(3)一氧化碳有毒,扩散到空气中会污染环境;
(4)化学反应前后,元素的种类不变,原子的种类、总个数不变;
不同的实验方法,有不同的优缺点.
解答:解:(1)为了获得干燥纯净的CO,A、B两装置中应分别存放氢氧化钠溶液、浓硫酸.
故填:氢氧化钠溶液.
(2)硬质玻璃管中发生反应的化学方程式为:Fe2O3+3CO
2Fe+3CO2.
故填:Fe2O3+3CO
2Fe+3CO2.
(3)选择图甲处理尾气,实验时应先点燃b处的酒精灯.理由是能够防止一氧化碳扩散到空气中;
图乙与图甲所示的尾气处理方法相比较,其主要优点是节约能源.
故填:b;能够防止一氧化碳扩散到空气中;节约能源.
(4)由CO+PdCl2+H2O═Pd↓+CO2+2R可知,每个R中含有1个氢原子和1个氯原子,是氯化氢,化学式为HCl;
此法与上述方法相比除了具有图乙比图甲所示方法的优点外,从实验角度看它还有的优点是安全、操作简单.
故填:HCl;安全、操作简单.
故填:氢氧化钠溶液.
(2)硬质玻璃管中发生反应的化学方程式为:Fe2O3+3CO
| ||
故填:Fe2O3+3CO
| ||
(3)选择图甲处理尾气,实验时应先点燃b处的酒精灯.理由是能够防止一氧化碳扩散到空气中;
图乙与图甲所示的尾气处理方法相比较,其主要优点是节约能源.
故填:b;能够防止一氧化碳扩散到空气中;节约能源.
(4)由CO+PdCl2+H2O═Pd↓+CO2+2R可知,每个R中含有1个氢原子和1个氯原子,是氯化氢,化学式为HCl;
此法与上述方法相比除了具有图乙比图甲所示方法的优点外,从实验角度看它还有的优点是安全、操作简单.
故填:HCl;安全、操作简单.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,下列说法正确的是( )
| A、甲醛是由碳原子和水分子构成的 |
| B、甲醛是由碳、氢、氧三种元素组成 |
| C、甲醛分子由碳原子、氢分子、氧原子构成 |
| D、1个甲醛分子由一个碳元素、二个氢元素、一个氧元素组成 |
化学已经渗透到社会发展的各个方面,在下列领域中哪些与化学科学发展密切相关:①环境保护,②能源开发利用,③新材料研制,④计算机应用软件的研发.( )
| A、只有①②③ | B、只有②③④ |
| C、只有①② | D、①②③④ |

 实验探究:物质化学反应前后,其总质量是否发生改变.
实验探究:物质化学反应前后,其总质量是否发生改变.