题目内容
人的胃液正常pH值在1.5到0.9之间,酸度过高就会换胃酸过多症,下列物质中不宜用作治疗胃酸过多症的药剂成分的是( )
| A、纯碱粉末 |
| B、纯碳酸氢钠粉末 |
| C、生石灰粉末 |
| D、氢氧化镁粉末 |
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:胃酸的主要成分是盐酸,治疗胃酸过多,所选药物既要能除去多余的胃酸,而且不能对身体有损伤.可以选择碱性稍弱的碱,或者能与盐酸反应的部分盐.
解答:解:A、碳酸钠粉末可以与盐酸反应产生二氧化碳和水,既能除去胃酸而且对身体无害,故可选用;
B、NaHCO3能与盐酸反应生成氯化钠、水和二氧化碳,能用来治疗胃酸过多症,故可选用;
C、氧化钙粉末溶于水生成氢氧化钙,能除去盐酸,但氧化钙粉末溶于水会放出大量热,容易烧伤身体,故不能用氧化钙;
D、氢氧化镁粉末可以和盐酸发生中和反应,对身体无毒无害,故可选用.
故选C.
B、NaHCO3能与盐酸反应生成氯化钠、水和二氧化碳,能用来治疗胃酸过多症,故可选用;
C、氧化钙粉末溶于水生成氢氧化钙,能除去盐酸,但氧化钙粉末溶于水会放出大量热,容易烧伤身体,故不能用氧化钙;
D、氢氧化镁粉末可以和盐酸发生中和反应,对身体无毒无害,故可选用.
故选C.
点评:本题考查酸的化学性质,解题时不但要考虑能和盐酸反应,还要针对具体情况,腐蚀性不能太强等,如本题所选物质必须不能损害身体.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
下列叙述中属于物理变化的是( )
| A、氧气在一定的条件下能够变成液态的形式 |
| B、氧气在一定条件下转变成液态形式 |
| C、铁在潮湿的空气中能够有铁锈生成 |
| D、铁在潮湿的空气中有铁锈生成 |
下列实验操作正确的是( )
A、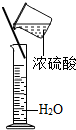 稀释浓硫酸 |
B、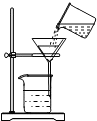 过滤 |
C、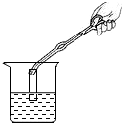 检测溶液的pH |
D、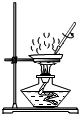 蒸发 |
某化肥中含NH4NO316%,若不考虑其他成分,则此化肥中含氮元素的质量分数为( )
| A、5.6% | B、10% |
| C、24% | D、27% |
在化学反应2Cl2+2Ca(OH)2=CaCl2+X+2H2O中,X的化学式为( )
| A、CaO |
| B、HCl |
| C、CaClO |
| D、Ca(ClO)2 |
下列各组物质,按单质、化合物、混合物顺序排列的是( )
| A、氢气、干冰、冰水共存物 |
| B、天然气、小苏打、烧碱 |
| C、液态氧、氯化氢、洁净的空气 |
| D、稀有气体、酒精、纯碱 |
我国在春秋战国时期就懂得将生铁经退火处理得到相当铸钢的器具(如锋利的宝剑),生铁退火处理的作用是( )
| A、除硫、磷杂质 |
| B、适当降低了含碳量 |
| C、渗透合金元素 |
| D、改造表面结构性质 |
将锌片分别插入下列各溶液中,反应后的溶液质量增加的是( )
①稀硫酸②硫酸铜③硝酸银④氯化镁.
①稀硫酸②硫酸铜③硝酸银④氯化镁.
| A、① | B、①② | C、①②③ | D、④ |