题目内容
 学校化学小组的同学用稀盐酸与石灰石(杂质不溶于水,也不与酸反应)反应制取40%的CaCl2溶液用于融雪.取105.4g稀盐酸,加入20g(足量)石灰石.反应过程如下:
学校化学小组的同学用稀盐酸与石灰石(杂质不溶于水,也不与酸反应)反应制取40%的CaCl2溶液用于融雪.取105.4g稀盐酸,加入20g(足量)石灰石.反应过程如下:| 反应时间(s) | t0 | t1 | t2 | t3 | t4 | t5 |
| 烧杯内物质质量(g) | 125.4 | 123.4 | 121.9 | 121.4 | 121 | 121 |
4.4
4.4
g.t3时溶液中的溶质是CaCl2和HCl
CaCl2和HCl
.(2)求t4时溶液的溶质质量分数.
(3)将t5时烧杯内物质过滤后,蒸发
83.3
83.3
g水,即可得到40%的CaCl2溶液.(4)请在座标图中画出生成气体的质量(m)g随时间(t)变化的曲线.
分析:(1)依据图标提供的数据可知烧杯中的盐酸完全反应时烧杯内物质质量是121g,所以t3时溶液中的盐酸有剩余;所以可依据t0~t4质量变化求出生成二氧化碳的质量;
(2)t4时依据二氧化碳的质量可以求出生成的氯化钙的质量和反应的碳酸钙的质量,进而可求此时的溶质质量分数;
(3)依据浓缩时溶质的质量不变,据此可求蒸发的水的质量;
(4)依据图表中的数据可分别求出不同温度下的生成二氧化碳的质量,依据描点法可以绘制出相应的曲线;
(2)t4时依据二氧化碳的质量可以求出生成的氯化钙的质量和反应的碳酸钙的质量,进而可求此时的溶质质量分数;
(3)依据浓缩时溶质的质量不变,据此可求蒸发的水的质量;
(4)依据图表中的数据可分别求出不同温度下的生成二氧化碳的质量,依据描点法可以绘制出相应的曲线;
解答:解:(1)依据图表数据可知当烧杯内物质质量是121g时(g)二氧化碳不会再生成,此时生成二氧化碳的质量=125.4g-121g=4.4g;所以t3时溶液中的盐酸有剩余,因此溶液中含有反应生成的氯化钙和氯化氢;
(2)设参加反应的CaCO3质量为x,生成CaCl2质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
=
=
x=10g y=11.1g
t4时溶液的溶质质量分数:
×100%=10%
(3)设蒸发掉质量是x的水后可得到40%的CaCl2溶液;
有以上分析可知t5时溶液的质量=105.4g+10g-4.4g=111g
(111g-x)×40%=111g×10%
x=83.3g
(4)采用描点法绘制即可 t0时生成的二氧化碳的质量为0;t1时生成的二氧化碳的质量为125.4g-123.4g=2g;t2时生成的二氧化碳的质量为125.4g-121.9=3.5g;t3时生成的二氧化碳的质量为125.4g-121.4=4g;t4时生成的二氧化碳的质量为125.4g-121=4.4g;t5时生成的二氧化碳的质量为125.4g-121=4.4g;
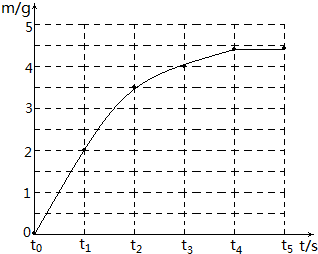
故答案为:(1)4.4;CaCl2和HCl;(2)答:t4时溶液的溶质质量分数10%;(3)83.3;(4) 如图
如图
(2)设参加反应的CaCO3质量为x,生成CaCl2质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
| 100 |
| x |
| 111 |
| y |
| 44 |
| 4.4g |
x=10g y=11.1g
t4时溶液的溶质质量分数:
| 11.1g |
| 105.4g+10g-4.4g |
(3)设蒸发掉质量是x的水后可得到40%的CaCl2溶液;
有以上分析可知t5时溶液的质量=105.4g+10g-4.4g=111g
(111g-x)×40%=111g×10%
x=83.3g
(4)采用描点法绘制即可 t0时生成的二氧化碳的质量为0;t1时生成的二氧化碳的质量为125.4g-123.4g=2g;t2时生成的二氧化碳的质量为125.4g-121.9=3.5g;t3时生成的二氧化碳的质量为125.4g-121.4=4g;t4时生成的二氧化碳的质量为125.4g-121=4.4g;t5时生成的二氧化碳的质量为125.4g-121=4.4g;

故答案为:(1)4.4;CaCl2和HCl;(2)答:t4时溶液的溶质质量分数10%;(3)83.3;(4)
 如图
如图点评:此题难度较大,解题的关键和突破口是依据质量守恒定律求出二氧化碳,据此分析解答相关问题即可,特别要注意的是求t4时溶液的溶质质量分数时溶液的质量不能使用121g,因为该质量中含有未反应的碳酸钙;

练习册系列答案
相关题目
 学校化学小组的同学用稀盐酸与石灰石(杂质不溶于水,也不与酸反应)反应制取40%的CaCl2溶液用于融雪.取105.4g稀盐酸,加入20g(足量)石灰石.反应过程如下:
学校化学小组的同学用稀盐酸与石灰石(杂质不溶于水,也不与酸反应)反应制取40%的CaCl2溶液用于融雪.取105.4g稀盐酸,加入20g(足量)石灰石.反应过程如下:
| 反应时间(s) | t0 | t1 | t2 | t3 | t4 | t5 |
| 烧杯内物质质量(g) | 125.4 | 123.4 | 121.9 | 121.4 | 121 | 121 |
(2)求t4时溶液的溶质质量分数.
(3)将t5时烧杯内物质过滤后,蒸发______g水,即可得到40%的CaCl2溶液.
(4)请在座标图中画出生成气体的质量(m)g随时间(t)变化的曲线.
学校化学小组的同学用稀盐酸与石灰石(杂质不溶于水,也不与酸反应)反应制取40%的CaCl2溶液用于融雪.取105.4g稀盐酸,加入20g(足量)石灰石.反应过程如下:
(1)反应共产生了CO2______g.t3时溶液中的溶质是______.
(2)求t4时溶液的溶质质量分数.
(3)将t5时烧杯内物质过滤后,蒸发______g水,即可得到40%的CaCl2溶液.
(4)请在座标图中画出生成气体的质量(m)g随时间(t)变化的曲线.
| 反应时间(s) | t | t1 | t2 | t3 | t4 | t5 |
| 烧杯内物质质量(g) | 125.4 | 123.4 | 121.9 | 121.4 | 121 | 121 |
(2)求t4时溶液的溶质质量分数.
(3)将t5时烧杯内物质过滤后,蒸发______g水,即可得到40%的CaCl2溶液.
(4)请在座标图中画出生成气体的质量(m)g随时间(t)变化的曲线.
