题目内容
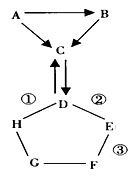
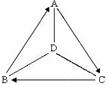
现有A、B、C、D四种物质分别是纯铁片、稀硫酸、碳酸钠溶液、氯化钡溶液中的一种,用四个六边形表示四种物质,用相邻的六边形有共同的边表示两种物质可以发生反应,请回答下列问题:(已知金属钡的金属活动性在钾和钙之间)
(1)A和B发生置换反应,B能和其他三种物质都反应,将C、D画在A和B周围的适当位置,在六边形中写出物质化学式或溶质的化学式,并注明物质的代号;
(2)写出产生白色沉淀的化学方程式 ;
(3)足量的A与B反应的实验现象为 。
(1)如下图(1分)(代号不标注,不扣分,合理给分)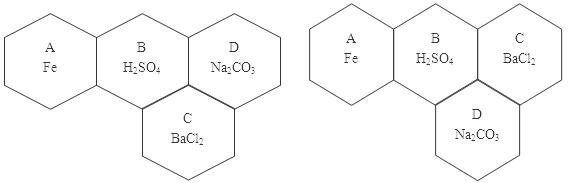
(2)Na2CO3 + BaCl2 =" 2NaCl" + Ba CO3↓(1分)
BaCl2 + H2SO4 = BaSO4↓+ 2HCl (沉淀符号使用错误不给分)(1分)
(3)银白色固体(逐渐)减少,(固体)表面产生气泡,放热,溶液由无色变为浅绿色。(1分)
解析试题分析:(1)A和B会发生置换反应,结合题中给出的四种物质,A和B是纯铁片和稀硫酸中的一种,B又能与其他三种物质反应,所以B是硫酸,A是纯铁片,硫酸、碳酸钠、和氯化钡三种物质两两之间都会发生反应,所以四种物质之间的图示可以表示成如下: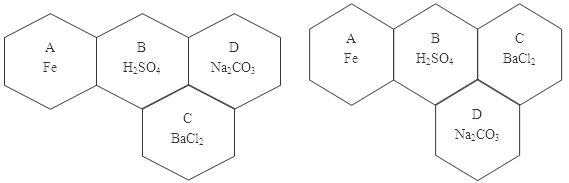
(2)在上面的反应中,碳酸钠和氯化钡反应生成白色的碳酸钡沉淀,氯化钡和硫酸反应生成白色的硫酸钡沉淀,方程式为:Na2CO3+BaCl2═2NaCl+BaCO3↓; BaCl2+H2SO4═BaSO4↓+2HCl;
(3)铁和硫酸反应时,铁逐渐的转化成可溶性的硫酸亚铁,硫酸亚铁显浅绿色,并且生成氢气,所以纯铁片和硫酸反应的现象是:银白色固体(逐渐)减少,(固体)表面产生气泡,放热,溶液由无色变为浅绿色。
考点:物质的鉴别、推断;金属的化学性质;酸的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式

 期末集结号系列答案
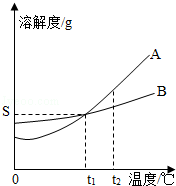
期末集结号系列答案下图为NaCl、KNO3的溶解度曲线,下列说法正确的是
| A.KNO3的溶解度一定大于NaCl溶解度 |
| B.20℃时,50g水最多能溶解31.6gKNO3 |
| C.t℃时,NaCl和KNO3的饱和溶液的溶质质量分数相等 |
| D.50℃的NaCl饱和溶液降温到20℃时变成不饱和溶液 |