题目内容
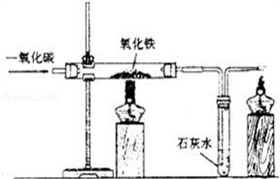
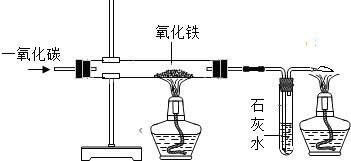
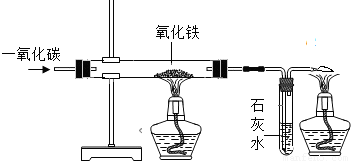
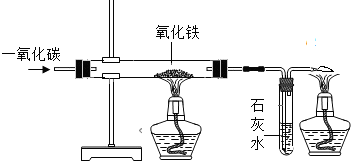
王浩同学在实验室中对炼铁原理进行了探究,请你帮助完成下列内容:(1)按照图示组装实验装置后,首先应______.
(2)在硬质玻璃管中放入少量______色的氧化铁粉末,先______同时点燃______处的酒精灯,然后点燃______处酒精灯.
(3)当______后,先关闭______处的酒精灯,待______后再停止通人CO,最后移走______处的酒精灯.
(4)该实验所发生的化学反应方程式______ 2Fe+3CO2
【答案】分析:只有熟悉一氧化碳与氧化铁反应的生成物、实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用等知识,才能正确解答本题.
解答:解:(1)对于有气体参加的反应,首先应该检查装置的气密性,查看装置是否漏气;
(2)氧化铁是一种红色粉末,先通入CO的目的是排净试管内的空气.因为CO有毒,不能直接排放到空气中去,所以应该把CO进行尾气处理转化为CO2,再进行加热;
(3)当红色氧化铁粉末完全变黑时,说明氧化铁已经完全反应,应先停止加热,继续通一氧化碳,直到试管冷却到室温后再停止通入CO,这样做的目的是为了防止生成的铁被空气中的氧气氧化,最后移走C处的酒精灯;
(4)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,该反应的化学方程式为:Fe2O3+3CO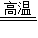 2Fe+3CO2;二氧化碳遇到石灰水变浑浊,该反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;在一氧化碳与氧化铁的反应中,CO中碳元素的化合价升高做还原剂,氧化铁中的铁元素化合价降低做氧化剂,发生还原反应;
2Fe+3CO2;二氧化碳遇到石灰水变浑浊,该反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;在一氧化碳与氧化铁的反应中,CO中碳元素的化合价升高做还原剂,氧化铁中的铁元素化合价降低做氧化剂,发生还原反应;
(5)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,二氧化碳能使澄清的石灰水变混浊,所以当澄清的石灰水变混浊说明有二氧化碳生成,也就可以判断反应已发生;CO有毒,不能排放到空气中去,所以C处酒精灯的作用是点燃未反应的CO,防止空气污染;
(6)如果不先通一氧化碳而是先给Fe2O3加热后通CO,这样就会造成试管内的空气没有排除,CO与空气混合可能达到爆炸极限,这样就会造成爆炸.
故答案为:(1)检查装置气密性;
(2)红色、通入CO、C、A;
(3)红色粉末完全变黑、A、冷却到室温、C;
(4)Fe2O3+3CO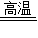 2Fe+3CO2,Ca(OH)2+CO2=CaCO3↓+H2OCO、Fe2O3;
2Fe+3CO2,Ca(OH)2+CO2=CaCO3↓+H2OCO、Fe2O3;
(5)石灰水变混浊;点燃未反应的CO,防止空气污染;
(6)先给Fe2O3加热,后通CO,未排净空气,CO与空气混合可能达到爆炸极限.
点评:本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用,难度稍大.
解答:解:(1)对于有气体参加的反应,首先应该检查装置的气密性,查看装置是否漏气;
(2)氧化铁是一种红色粉末,先通入CO的目的是排净试管内的空气.因为CO有毒,不能直接排放到空气中去,所以应该把CO进行尾气处理转化为CO2,再进行加热;
(3)当红色氧化铁粉末完全变黑时,说明氧化铁已经完全反应,应先停止加热,继续通一氧化碳,直到试管冷却到室温后再停止通入CO,这样做的目的是为了防止生成的铁被空气中的氧气氧化,最后移走C处的酒精灯;
(4)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,该反应的化学方程式为:Fe2O3+3CO
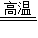 2Fe+3CO2;二氧化碳遇到石灰水变浑浊,该反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;在一氧化碳与氧化铁的反应中,CO中碳元素的化合价升高做还原剂,氧化铁中的铁元素化合价降低做氧化剂,发生还原反应;
2Fe+3CO2;二氧化碳遇到石灰水变浑浊,该反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;在一氧化碳与氧化铁的反应中,CO中碳元素的化合价升高做还原剂,氧化铁中的铁元素化合价降低做氧化剂,发生还原反应;(5)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,二氧化碳能使澄清的石灰水变混浊,所以当澄清的石灰水变混浊说明有二氧化碳生成,也就可以判断反应已发生;CO有毒,不能排放到空气中去,所以C处酒精灯的作用是点燃未反应的CO,防止空气污染;
(6)如果不先通一氧化碳而是先给Fe2O3加热后通CO,这样就会造成试管内的空气没有排除,CO与空气混合可能达到爆炸极限,这样就会造成爆炸.
故答案为:(1)检查装置气密性;
(2)红色、通入CO、C、A;
(3)红色粉末完全变黑、A、冷却到室温、C;
(4)Fe2O3+3CO
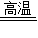 2Fe+3CO2,Ca(OH)2+CO2=CaCO3↓+H2OCO、Fe2O3;
2Fe+3CO2,Ca(OH)2+CO2=CaCO3↓+H2OCO、Fe2O3;(5)石灰水变混浊;点燃未反应的CO,防止空气污染;
(6)先给Fe2O3加热,后通CO,未排净空气,CO与空气混合可能达到爆炸极限.
点评:本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用,难度稍大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 王浩同学在实验室中对炼铁原理进行了探究,请你帮助完成下列内容:
王浩同学在实验室中对炼铁原理进行了探究,请你帮助完成下列内容: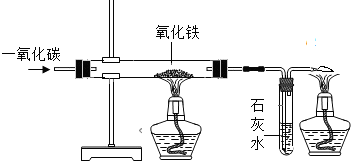 王浩同学在实验室中对炼铁原理进行了探究,请你帮助完成下列内容:
王浩同学在实验室中对炼铁原理进行了探究,请你帮助完成下列内容: