题目内容
如何除去硫酸亚铁中混有的少量杂质硫酸铜?请写出操作过程和有关的化学方程式.
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据主要物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:硫酸铜和硫酸亚铁的酸根离子相同,金属活动性有差异,要除去硫酸铜杂质,又不能在硫酸亚铁中引入新的杂质,可以利用铁跟硫酸铜反应,将硫酸铜转化为硫酸亚铁的方法进行除杂.
具体操作如下:①把混有少量硫酸铜杂质的硫酸亚铁溶解于水;②向溶液中加入过量的Fe粉;③充分反应后,过滤,滤渣是铜和铁的混合物,滤液是硫酸亚铁溶液;④经过蒸发、浓缩可以得到硫酸亚铁晶体.
铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═Cu+FeSO4.
故答案为::①把混有少量硫酸铜杂质的硫酸亚铁溶解于水;②向溶液中加入过量的Fe粉;③充分反应后,过滤,滤渣是铜和铁的混合物,滤液是硫酸亚铁溶液;④经过蒸发、浓缩可以得到硫酸亚铁晶体.
Fe+CuSO4═Cu+FeSO4.
具体操作如下:①把混有少量硫酸铜杂质的硫酸亚铁溶解于水;②向溶液中加入过量的Fe粉;③充分反应后,过滤,滤渣是铜和铁的混合物,滤液是硫酸亚铁溶液;④经过蒸发、浓缩可以得到硫酸亚铁晶体.
铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═Cu+FeSO4.
故答案为::①把混有少量硫酸铜杂质的硫酸亚铁溶解于水;②向溶液中加入过量的Fe粉;③充分反应后,过滤,滤渣是铜和铁的混合物,滤液是硫酸亚铁溶液;④经过蒸发、浓缩可以得到硫酸亚铁晶体.
Fe+CuSO4═Cu+FeSO4.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
下列关于镁原子和镁离子叙述正确的是( )
| A、它们的核外电子数相同 |
| B、它们都是电中性的粒子 |
| C、它们都具有相同的质子数,是同种元素 |
| D、镁原子得到电子后变成镁离子 |

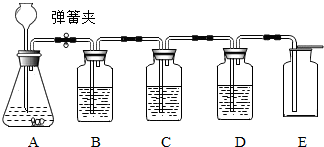

 氢氧化钠是一种重要的化工原料,工业上常用点解饱和食盐水的方法来制取烧碱,并生成氯气(Cl2)和氢气.
氢氧化钠是一种重要的化工原料,工业上常用点解饱和食盐水的方法来制取烧碱,并生成氯气(Cl2)和氢气.