题目内容
【题目】鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小勇同学进行了如下实验。请回答相关问题:
(1)他将蛋壳洗净、干燥并捣碎放在烧杯里,然后往烧杯中加入足量盐酸,在蛋壳上看到的现象是_____________。
(2)实验过程和测定的相关实验数据如下所示:
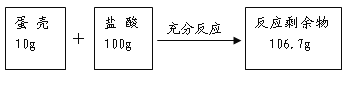
①实验过程中产生二氧化碳的质量为_______ g。
②小勇同学求出了蛋壳中碳酸钙的质量分数,请你写出小勇的计算过程___________________。
【答案】 有气泡产生 3.3g 75%
【解析】(1) 鸡蛋壳的主要成分是碳酸钙,加入足量盐酸后会产生二氧化碳;(2)反应前后减少的质量是二氧化碳的质量,二氧化碳被石灰水完全吸收后,石灰水增加的质量也是二氧化碳的质量,CO2的质量=10g+100g-106.7g=3.3g;
设鸡蛋壳中碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
![]()
x=7.5g,
碳酸钙的质量分数为: ![]() ×100%=75%。
×100%=75%。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目